1、选择题 如下图所示,晶体中每个来源:91考试网 91Exam.org阳离子A或阴离子B,均可被另一种离子以四面体形式包围着,则该晶体对应的化学式为
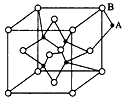
[? ]
A.AB
B.A2B
C.AB3
D.A2B3
参考答案:A
本题解析:
本题难度:一般
2、选择题 下列关于晶体的说法正确的组合是(? )
① 分子晶体中都存在共价键?
② 在晶体中只要有阳离子就一定有阴离子
③ 金刚石、SiC、NaF、NaCl、H2O、H2S晶体的熔点依次降低?
④ 离子晶体中只有离子键没有共价键,分子晶体中肯定没有离子键?
⑤ 氯化钠熔化时离子键被破坏
⑥ SiO2晶体中每个硅原子与两个氧原子以共价键相结合?
⑦ 晶体中分子间作用力越大,分子越稳定?
A.①②③⑥? B.①②④? C.③⑤⑥? D.③⑤
参考答案:D
本题解析:略
本题难度:简单
3、选择题 下列物质的沸点(或固体的熔点)前者高于后者的是( )
A.新戊烷、异戊烷
B.苯酚、苯酚钠
C.乙酸、丙酸
D.硬脂酸和油酸
参考答案:A、新戊烷、异戊烷互为同分异构体,支链越多,沸点越低,则沸点前者小于后者,故A错误;
B、苯酚为分子晶体,苯酚钠为离子晶体,离子晶体的沸点高于分子晶体的沸点,则沸点前者小于后者,故B错误;
C、同系物中含有的碳原子个数越多,沸点越高,丙酸中碳原子数多,沸点高,则沸点前者小于后者,故C错误;
D、因分子晶体中,相对分子质量大的沸点高,硬脂酸(C17H35COOH)的相对分子质量大于油酸(C17H33COOH),故D正确;
故选D.
本题解析:
本题难度:简单
4、填空题 (三选一----物质结构与性质)
纳米技术制成的金属燃料、非金属固体燃料、氢气等已应用到社会生活和高科技领域。
(1)A和B的单质单位质量的燃烧热大,可用作燃料。已知A和B为短周期元素,其原子的第一至第四电离能如下表所示
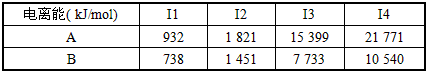
某同学根据上述信息,推断B的核外电子排布如图所示,
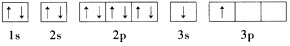
该同学所画的电子排布图违背了______________。
(2)ACl2分子中A的杂化类型为____________。
(3)氢气作为一种清洁能源,必须解决它的储存问题,C60可用作储氢材料。已知金刚石中的C-C的键长为154.45pm,C60中C-C键长为145~140pm,有同学据此认为C60的熔点高于金刚石,你认为是否正确________,并阐述理由_____________?。
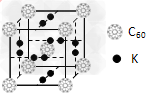
(4)科学家把C60和钾掺杂在一起制造了一种富勒烯化合物,?其晶胞如图所示,该物质在低温时是一种超导体。写出基态钾原子的价电子排布式____________,该物质的K原子和C60分子的个数比为________________。
(5)继C60后,科学家又合成了Si60、N60,C、Si、N原子电负性由大到小的顺序是___________,NCl3分子的VSEPR模型为?__________。Si60分子中每个硅原子只跟相邻的3个硅原子形成共价键,且每个硅原子最外层都满足8电子稳定结构,则Si60分子中π键的数目为_____________?。
参考答案:(1)能量最低原理?
(2)sp杂化
(3)否 ;C60为分子晶体,熔化时破坏的是分子间作用力,无需破坏共价键
(4)4s1 ;3:1
(5)N>C>Si ;正四面体 ;30
本题解析:
本题难度:一般
5、选择题 下列叙述正确的是
A.正四面体构型的分子中键与键之间的夹角均是109°28′
B.粒子间以分子间作用力结合而成的晶体其熔点一般不会很高
C.离子晶体中含有离子键,不能含有共价键
D.金属阳离子只能存在于离子晶体中
参考答案:B
本题解析:白磷P4也是正四面体构型,其键角为60°,A项错误;以分子间作用力结合的晶体为分子晶体,分子晶体的熔沸点低,B项正确;离子晶体中一定含有离子键,可能含有共价键,C项错误;金属阳离子还可能存在金属晶体中,D项错误。答案选B。
点评:四原子形成的正四面体构型键角60°,五原子形成的正四面体构型键角109°28′。
本题难度:一般