1��ѡ���� ���������У�������ԭ�ӻ�����������㶼Ϊ8���ӽṹ����
[? ]
A��HCl
B��Na2S
C��LiCl
D��H2O
�ο��𰸣�B
���������
�����Ѷȣ���
2��ѡ���� A��B��C��D���Ƕ�����Ԫ�أ�ԭ�Ӱ뾶��D��C��A��B����֪��A��Bͬ���ڣ�A��C����ͬһ���壻Cԭ�Ӻ��ڵ�����������A��Bԭ�Ӻ��ڵ�������֮�ͣ�Cԭ��������������Dԭ��������������5��������˵������ȷ���ǣ�������
A��A��C��Ԫ�ؿ��ܴ��ڵڢ�A���ڢ�A��
B��D��B��Ԫ����ɵ��������ӻ�������������������֮��Ϊ2��1��1��1
C������Ԫ�صļ����ӵİ뾶��С˳��Ϊ��C��D��B
D��D��C��B����Ԫ����ɵĻ�����Ļ�ѧʽΪDCB2
�ο��𰸣�A��B��C��D���Ƕ�����Ԫ�أ�ԭ�Ӱ뾶��D��C��A��B����֪��A��Bͬ���ڣ�A��C����ͬһ���壬A��B��C�����λ��Ϊ
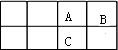
��Cԭ�Ӻ��ڵ�����������A��Bԭ�Ӻ��ڵ�������֮�ͣ���A��������Ϊx����B��������Ϊx+1��C��������Ϊx+8����x+x+1=x+8�����x=7����AΪN��BΪO��CΪP��Cԭ��������������Dԭ��������������5������D����������Ϊ1�����ԭ�Ӱ뾶��֪DӦΪNa��
A��A��C��Ԫ�ش��ڵڢ�A�壬��A����
B��D��B��Ԫ����ɵ��������ӻ�����ΪNa2O��Na2O2��������������֮�Ⱦ�Ϊ1��2����B����
C��D��B�����Ӿ�����ͬ�����Ų���ԭ������������Ӱ뾶С��C�����ӵ��Ӳ���࣬���Ӱ뾶���������Ԫ�صļ����ӵİ뾶��С˳��Ϊ��C��B��D����C����
D��DΪNa�����Ϊ+1�ۣ�BΪO����ͼ�Ϊ-2�ۣ���D��C��B����Ԫ����ɵĻ�����Ļ�ѧʽΪDCB2����C�Ļ��ϼ�Ϊ+3�ۣ�����ʵ��С�����+5�ۣ���D��ȷ��
��ѡD��
���������
�����Ѷȣ���
3��ѡ���� �йػ�ѧ������ȷ���ǣ�������
���ǻ��ĵ���ʽ?
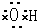
?����ϩ�Ľṹ��ʽ��CH2CH2]������ĵ���ʽ
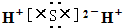
?�ܱ�����ӵ����ģ�ͣ�
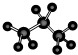
�ݱ����ӵı���ģ��?

?����Ľṹʽ?
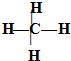
A���٢�
B���ڢۢ�
C���ܢݢ�
D���ڢۢ�
�ο��𰸣�C
���������
�����Ѷȣ���
4�������� ���ʽṹ���������������������ʱ仯�ı��ʣ����з�����ƺ��о���Ӧ���ɡ���ش��������⣺
��1���������ڻ�̬ԭ����2��δ�ɶԵ����ҵ縺������Ԫ����_____��
��2�����������ܵ���������ʱ�����α䣬�����Ӿ����������ѡ��Դӽṹ�ĽǶȷ������е���Ҫԭ��____________��
��3����֪��ˮ�д���ƽ��2H2O��H3O����OH�������з����У�����ԭ�Ӳ�ȡ���ӻ���ʽ��H3O+����ԭ�ӵ��ӻ���ʽ��ͬ����_____
a.CH2=CH2�е�̼ԭ��? b.NH2���еĵ�ԭ��
c.ClO3���е���ԭ��? d.NO2���еĵ�ԭ��
��4��F��Mg��K����Ԫ���γɵľ��徧���ṹ��ͼ��ʾ��һ��������MgԪ�ص���������Ϊ________��
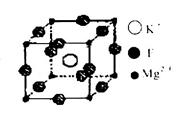
�ο��𰸣���1��S������ǣ���1�֣� ��2�������������ɽ��������Ӻ͡����ɵ��ӡ�ͨ���������γɵIJ�״���ܶѻ��ṹ��1�֣�������������������ʱ�����������и�ԭ�Ӳ�ᷢ����Ի����������α䣬���ɵ���ʹ�ø���֮��ʼ�ձ����Ž����������ã�1�֣������Ӿ����������������Ӽ�����ž������ã�ʹ�������Ӳ��ܷ��������ƶ�������ܵ���������ʱ���Ӽ����ƻ���ʹ�������ѣ�1�֣�
��3��bc��2�֣� ��4��20%��2�֣�
�����������1���������ڻ�̬ԭ���к�������δ�ɶԵ��ӵ�Ԫ����Si��S����Ԫ�أ�ͬһ�����У�Ԫ�صĵ縺������ԭ���������������������Si�ĵ縺��С��SԪ�ء�
��2����������Ĺ������ǽ��������Ӻ����ɵ��ӣ����ڵ��������ǽ������������������ɽ��������Ӻ����ɵ���ͨ���������γɵIJ�״���ܶѻ��ṹ������������������ʱ�����������и�ԭ�Ӳ�ᷢ����Ի����������α䣬���ɵ���ʹ�ø���֮��ʼ�ձ����Ž����������ã����Ӿ����д��ڵ������������ӣ����ڵ������������Ӽ������Ӿ����������������Ӽ�����ž������ã�ʹ�������Ӳ��ܷ��������ƶ�������ܵ���������ʱ���Ӽ����ƻ���ʹ�������ѡ�
��3��H3O+��������ԭ�Ӻ���3���Ҽ���һ���µ��Ӷԣ�������۲���Ӷ�����4������ԭ�Ӳ�ȡsp3�ӻ���a��CH2�TCH2�е�ÿ��̼ԭ�Ӻ���3���Ҽ��Ҳ����µ��Ӷԣ����Բ�ȡsp2�ӻ����ʴ���b��NH2���еĵ�ԭ�Ӻ���2���Ҽ��ͣ�5��1��2��1����2��2���µ��Ӷԣ����Ե�ԭ�Ӳ�ȡsp3�ӻ�����b��ȷ��c��ClO3���е���ԭ�Ӻ���3���Ҽ��ͣ�7��1��3��2����2��1���µ��Ӷԣ�������۲���Ӷ�����4������ԭ�Ӳ�ȡsp3�ӻ�����c��ȷ��d��NO2���еĵ�ԭ�Ӻ���2���Ҽ��ͣ�5��1��2��2����2��1���µ��Ӷԣ�������۲���Ӷ�����3�����Ե�ԭ�Ӳ�ȡsp2�ӻ�����d������˴�ѡbc��
��4�����ݾ����ṹ�����ݾ�̯����֪���þ����к���þԭ�Ӹ�����8��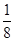 ��1����ԭ�Ӹ�����1����ԭ�Ӹ�����12��
��1����ԭ�Ӹ�����1����ԭ�Ӹ�����12��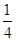 ��3�������仯ѧʽΪKMgF3����˸û�������þԪ�ص�����������
��3�������仯ѧʽΪKMgF3����˸û�������þԪ�ص�����������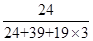 ��100%��20%��
��100%��20%��
�����Ѷȣ�һ��
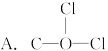
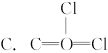
5��ѡ���� ��֪����(COCl2)�ķ��ӽṹ�У���ԭ�ӵ��������Ӿ�����8�����ȶ��ṹ����������ӵĽṹʽ��ȷ����(?)
 ?
?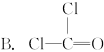
 ?D.Cl��C��O��Cl
?D.Cl��C��O��Cl
�ο��𰸣�B
�������������һ��Ҫ���жϷ����ڲ��ṹ����Ŀ���жϵ������Ǹ�ԭ�ӵ��������Ӿ�������8�����ȶ��ṹ���ݴ˿�֪������ԭ��Ӧ�ɼ�����Ŀ����C��O��Clԭ�������ֱ���4��6��7�����ӣ�Ҫ�ﵽ�ȶ��ṹ������ɼ�����ĿΪ4��2��1��
�����Ѷȣ���