1、选择题 在2A+B 3C+4D反应中,下面表示的反应速率最快的是(?)
3C+4D反应中,下面表示的反应速率最快的是(?)
A.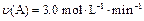
B.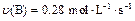
C.
D.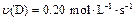
参考答案:B
本题解析:略
本题难度:简单
2、填空题 合成氨反应N2(g)+3H2(g) 2NH3(g),反应过程的能量变化如图所示。已知N2(g)与H2(g)反应生成17 g NH3(g),放出46.1 kJ的热量。
2NH3(g),反应过程的能量变化如图所示。已知N2(g)与H2(g)反应生成17 g NH3(g),放出46.1 kJ的热量。
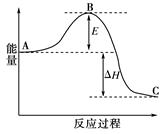
请回答下列问题:
(1)该反应通常用铁作催化剂,加催化剂会使图中E变_____(填“大”或“小”),E的大小对该反应的反应热有无影响?_ _。理由是_________ ;
(2)图中ΔH=________kJ・mol-1;
(3)起始充入2mol・L-1 N2和5.5 mol・L-1 H2,经过50 min,NH3的浓度为1mol・L-1,
则v(N2)=____________mol・L-1・min-1、C(H2)=______________mol・L-1;
已知NH3(g)= NH3 (l) ΔH=-QkJ・mol-1,书写N2(g)+3H2(g)=2NH3 (l)的热化学方程式 ________ 。
参考答案:(1)小,无。△H取决于反应物的总能量和生成物的总能量差;(2)-92.2 (3)0.01 4
(4)N2(g) + 3H2(g) ? 2NH3(g) ΔH=-(92.2+Q)kJ・mol-1
本题解析:(1)用铁作催化剂可以降低反应活化能E,所以加催化剂会使图中E变变小;△H取决于反应物的总能量和生成物的总能量差,所以E的大小对该反应的反应热没有影响。
(2)NH3的物质的量为17g/17g・mol-1="1mol" △H="2×-46.1" kJ="-92.2" kJ(该反应为放热反应,符号为负)
(3)NH3的变化浓度为1mol・L-1时,根据反应比,N2的浓度变化了0.5mol・L-1,v(N2)=0.5mol・L-1/50 min="0.01" mol・L-1;NH3的变化浓度为1mol・L-1时,根据反应比,H2的浓度变化了1.5 mol・L-1,C(H2)=5.5 mol・L-1-1.5 mol・L-1="4" mol・L-1
(4)N2(g) + 3H2(g) ? 2NH3(g) ΔH=-(92.2+Q)kJ・mol-1
考点:本题着重考查了化学反应热、化学反应速率计算的相关知识。
本题难度:一般
3、选择题 将4mol A气体和2mol B气体在2L的容器中混合并在一定条件下发生如下反应:2A(g)+B(g) 2C(g)若经2s后测得C的浓度为0.6mol
2C(g)若经2s后测得C的浓度为0.6mol
参考答案:
本题解析:
本题难度:一般
4、选择题 可逆反应 2A (气) + 3B (气)  ?2C (气) + D(气),在四种不同条件下反应速率最快的是
?2C (气) + D(气),在四种不同条件下反应速率最快的是
A.VA = 0.5mol/(L・min)
B.VB = 0.6mol/(L・min)
C.VC = 0.35mol/(L・min)
D.VD = 0.4mol/(L・min)
参考答案:D
本题解析:同一个化学反应,用不同的物质表示其反应速率时,数值可能不同,但表示的意义是相同的。所以在比较反应速率快慢时,应该换算成用同一种物质表示,然后才能直接比较速率数值大小。根据速率之比是相应化学计量数之比可知,如果都用A表示反应速率,则分别是0.5mol/(L・min)、0.4mol/(L・min)、0.35mol/(L・min)、0.8mol/(L・min),所以答案选D。
本题难度:简单
5、选择题 下列相关实验的现象或结论正确的是
A.向NaAlO2溶液中滴入NaHCO3溶液有白色沉淀,则AlO2-结合质子能力比CO32-强
B.向少量的稀溴水中滴入饱和苯酚溶液立即产生白色沉淀
C.检验废铁屑溶于盐酸后所得的溶液中是否含有Fe2+,可向其中加入酸性KMnO4溶液,根据其是否褪色进行判断
D.加入硫酸铜可使锌与稀硫酸的反应速率加快,说明Cu2+具有催化作用