1、选择题 实验室区别下列物质选用的试剂(括号中的为试剂,必要时可加热)不正确的是( )
A.苯和己烯(溴水)
B.矿物油和植物油(NaOH溶液)
C.淀粉和纤维素(碘水)
D.硝基苯和CCl4(水)
参考答案:D
本题解析:己烯和溴水发生加成反应而碳酸,苯和溴水不反应,A正确。矿物油一般是碳氢化合物,植物油是油脂和氢氧化钠发生水解反应,B正确。碘遇淀粉显蓝色,C正确。硝基苯和CCl4均不溶于水,且密度都大于水的,因此选项D错误,所以答案是D。
本题难度:一般
2、填空题 下表中括号内的物质是杂质,试将除杂试剂和分离方法填入表中:
混合物
除杂试剂
分离方法
SiO2 (Fe2O3)
?
?
SiO2 (NaCl)
?
?
SiO2 (Si)
参考答案:
混合物
除杂试剂
分离方法
SiO2 (Fe2O3)
盐酸
过滤
SiO2 (NaCl)
水
过滤
SiO2 (Si)
O2
加热
本题解析:
本题难度:一般
3、选择题 已知苯(C6H6)通常是无色液体,不溶于水,密度小于1g?mL-1,沸点约为80.1℃.要从水与苯的混合物中将苯分离出来,下列方法中最为合理的是( )
A.蒸馏
B.分液
C.过滤
D.蒸发
参考答案:水与苯互不相溶,混合后会分层,互不相溶的两层液体分开要采用分液法,
故选B.
本题解析:
本题难度:简单
4、实验题 氯酸镁[Mg(ClO3)2]常用作催熟剂、除草剂等,实验室制备少量Mg(ClO3)2・6H2O的流程如下:
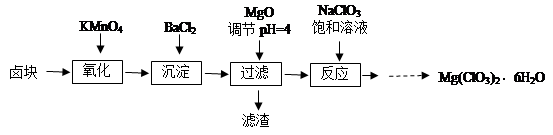
已知:①卤块主要成分为MgCl2・6H2O,含有MgSO4、FeCl2等杂质。
②四种化合物的溶解度(S )随温度(T )变化曲线如图所示。
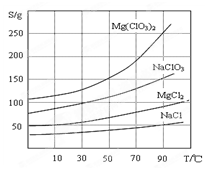
(1)过滤所需要的主要玻璃仪器有?。
(2)加入BaCl2的目的是?,加MgO后过滤所得滤渣的主要成分为?。
(3)加入NaClO3饱和溶液后发生反应的化学方程式为?
(4)产品中Mg(ClO3)2・6H2O含量的测定:
步骤1:准确称量3.50 g产品配成100 mL溶液。
步骤2:取10.00 mL于锥形瓶中,加入10.00 mL稀硫酸和20 .00mL 1.000 mol・L-1的FeSO4溶液,微热。
步骤3:冷却至室温,用0.100 mol・L-1 K2Cr2O7?溶液滴定剩余的Fe2+至终点,此过程中反应的离子方程式为:Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O。
步骤4:将步骤2、3重复两次,平均消耗K2Cr2O7?溶液15.00 mL。
①写出步骤2中发生反应的离子方程式:?;
②产品中Mg(ClO3)2・6H2O的质量分数为?。
参考答案:(1)漏斗、玻璃棒、烧杯?
(2)除去SO42-? BaSO4和Fe(OH)3
(3)MgCl2+2NaClO3=Mg(ClO3)2+2NaCl↓(未写沉淀符号不给分)?
(4)①ClO3-?+6Fe2++6H+=6Fe3++Cl-+3H2O?②78.3%
本题解析:(1)过滤所需要的主要玻璃仪器有漏斗、玻璃棒、烧杯;(2)加入BaCl2的目的是使杂质SO42-转化为沉淀除去。加MgO调整溶液的PH到4,这时Fe3+会形成Fe(OH)3沉淀.连同加入BaCl2后产生的硫酸钡沉淀一起过滤出去。所以过滤所得滤渣的主要成分为BaSO4和Fe(OH)3。(3)加入NaClO3饱和溶液后发生反应的化学方程式为MgCl2+2NaClO3=Mg(ClO3)2+2NaCl↓。从Mg(ClO3)2的溶液中得到Mg(ClO3)2・6H2O可利用其溶解度较大受温度的影响变化较大的特点先蒸发结晶;再趁热过滤;最后冷却结晶得到。(4)利用氧化还原反应中氧化剂得到的电子与还原剂失去的电子数相等来进行计算。①写出步骤2中发生反应的离子方程式:ClO3-?+6Fe2++6H+=6Fe3++Cl-+3H2O。②在10.00 mL溶液中1×0.02=3×2×0.015×0.1+ 6×n(ClO3-?).解得n(ClO3-?)="(" 0.011/6)mol.所以3.50 g产品中含有的Mg(ClO3)2・6H2O质量为{( 0.011/6)mol÷2}×10×299g/mol=2.741g.所以产品中Mg(ClO3)2・6H2O的质量分数为(2.741g÷3.50 g)×100%=78.3%3)2]的制取及成分测定的知识。
本题难度:一般
5、实验题 海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
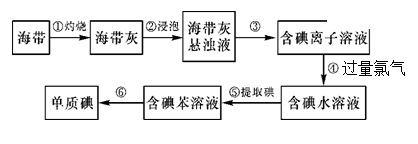
请填写下列空白:
(1)步骤①灼烧海带时,除需要三脚架、泥三角外,还需要用到的实验仪器是?
A.烧杯? B.表面皿? C.坩埚? D.酒精灯? E.圆底烧瓶
(2)请写出步骤④中反应的离子方程式:?
(3)步骤⑥是从含碘的苯溶液中分离出单质碘和回收苯,还需经过蒸馏,指出并改正下列实验装置中的错误之处(至少两处)。
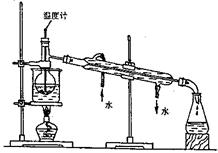
①?
②?
(4)步骤⑤中,某学生选择用苯来提取碘,其验操作可分解为如下几步:
(A)把盛有溶液的分液漏斗放在铁架台的铁圈中;
(B)把50毫升碘水和15毫升苯加入分液漏斗中,并盖好玻璃塞;
(C)检验分液漏斗活塞和上口的玻璃塞是否漏液;
(D)倒转漏斗用力振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正;
(E)旋开活塞,用烧杯接收溶液;
(F)将分液漏斗上口倒出上层溶液;
(G)将漏斗上口的玻璃塞打开或使塞上的凹槽或小孔对准漏斗口上的小孔;
(H)静置,分层。就此实验,完成下列填空:
①正确操作步骤的顺序是 ?→?→ ?→A→G→?→E→F
②上述(G)步骤操作的目的是?
③能选用苯从碘水中萃取碘的原因是?
参考答案:(1)C? D(2分)?(2)2I?―+Cl2=I2+2Cl_(2分)
(3)①温度计水银球位置没有放在蒸馏烧瓶的支管口。正确做法应将温度计水银球的上限与蒸馏烧瓶支管口的下限对齐。
②冷凝管中的水流方向错误。正确做法应是上进下出
③烧杯不能直接加热。正确做法应该垫上石棉网(任写两处,共4分)
(4)① C ?→? B?→ ?D →A→G→? H?→E→F(2分)
②与大气相通,使液体顺利流下(2分)
③苯与水互不相溶且不反应;I2在苯中溶解度比在水中的大;苯与碘互不反应。(2分,漏写一点给扣1分,错写或漏写两点以上不给分)
本题解析:(1)灼烧是在高温下进行的,因此选用坩埚来作反应的容器。除了坩埚,还得选用酒精灯。?(2)步骤④是用氯气将溶液中的碘离子置换成碘单质:2I?―+Cl2=I2+2Cl-(2分)
(3)①若像装置中这样插入液体中,测的是反应液的温度,温度计水银球位置没有放在蒸馏烧瓶的支管口。正确做法应将温度计水银球的上限与蒸馏烧瓶支管口的下限对齐。。
②为保证冷凝效果,冷凝管中的水流方向错误。正确做法应是上进下出,。
③为防止炸裂烧杯,烧杯不能直接加热。正确做法应该垫上石棉网,。
(4)① C ?→? B?→ ?D →A→G→? H?→E→F(2分)
②与大气相通,使液体顺利流下(2分)
③苯与水互不相溶且不反应;I2在苯中溶解度比在水中的大;苯与碘互不反应
本题难度:一般