1、简答题 X,Y,A,B,C,D是中学化学教材中常见的物质,且有图示的转化关系.气体C的式量比气体X的式量大2,D的焰色反应呈黄色,产物中水已忽略.
(1)写出有关物质的化学式:X______,Y______,D______.
(2)反应①的反应类型是(填基本反应类型)______.
(3)反应②的化学方程式为:______.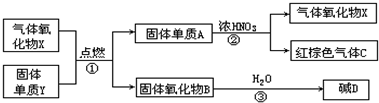
参考答案:X,Y,A,B,C,D是中学化学教材中常见的物质,题干转化关系中固体A和浓硝酸反应生成气体氧化物X和红棕色气体C,可以判断C为NO2,气体C的式量比气体X的式量大2,A为C,X为CO2;固体氧化物B溶于水生成碱D,说明B是金属氧化物,结合D的焰色反应呈黄色,证明D为NaOH,氧化物B为Na2O,依据转化关系可以推断,气体氧化物X为CO2,固体y为Na;
(1)依据推断X的化学式为:CO2;Y的化学式为:Na;D:NaOH;故答案为:CO2 Na;NaOH;
(2)反应①是4Na+CO2=C+2Na2O;发生的反应类型是置换反应,故答案为:置换反应;
(3)反应②是碳和浓硝酸的反应生成二氧化碳、二氧化氮和水,反应的化学方程式为:C+4HNO3?△?.?CO2↑+4NO2↑+2H2O;故答案为:C+4HNO3?△?.?CO2↑+4NO2↑+2H2O;
本题解析:
本题难度:一般
2、填空题 下图是无机物A~M在一定条件下的转化关系(部分产物及反应条件未列出)。其中,I是由第三周期元素组成的单质中熔点最高的金属,K是一种红棕色气体。
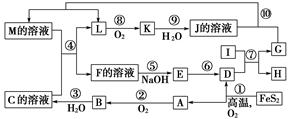
提示:4FeS2+11O2高温,2Fe2O3+8SO2
请填写下列空白:
(1)在周期表中,组成单质G的元素位于第________周期________族。
(2)在反应⑦中氧化剂与还原剂的物质的量之比为________。
(3)在②、③、⑥、⑨中既属于化合反应又属于非氧化还原反应的是________(填序号)。
(4)反应④的离子方程式是_____________________________________。
(5)将化合物D与KNO3、KOH共熔,可制得一种“绿色”环保高效净水剂K2FeO4(高铁酸钾),同时还生成KNO2和H2O。该反应的化学方程式是________________________。
参考答案:(1)四 Ⅷ
(2)1∶2
(3)③
(4)3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O
(5)Fe2O3+3KNO3+4KOH=2K2FeO4+3KNO2+2H2O
本题解析:该题推断的突破口是反应①,根据“提示”可知D、A分别是Fe2O3、SO2;根据题中叙述信息,可知I为Al,K为NO2,再根据框图信息可以推断出B为SO3,C为硫酸,E为Fe(OH)3,F的溶液中含Fe3+,G为Fe,H为氧化铝,J为硝酸,L为NO,M的溶液中含Fe2+。
本题难度:困难
3、推断题 已知B是一种由三种短周期(各位于不同周期)元素组成的正盐,该盐在常用锌锰干电池中做电解质;Y在常温下为液态,E的相对分子质量比D大16,它们存在如下转化关系(反应条件及部分产物已略去)
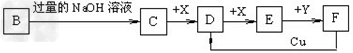
请回答下列问题: ?
(1)B的化学式为_____________;F与Cu反应的离子方程式为_________;
(2)C可与过量的Cl2反应生成HCl和物质A,A可发生水解反应生成NH3和HClO,则C与过量Cl2反应的化学方程式为___________,反应中的还原剂为___________;
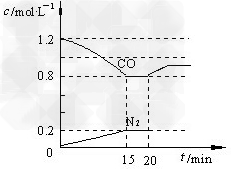
(3)D气体和CO都是汽车尾气的主要成分,降低汽车尾气的方法之一是在排气管上安装催化转化器,发生如下反应:2D(g)?+?2CO(g)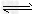 N2(g)?+?2CO2(g);△H<0。若在一定温度下,将1.4?mol?D、1.2?mol?CO充入1?L固定容积的容器中,反应过程中各物质的浓度变化如图所示。
N2(g)?+?2CO2(g);△H<0。若在一定温度下,将1.4?mol?D、1.2?mol?CO充入1?L固定容积的容器中,反应过程中各物质的浓度变化如图所示。
①该反应的化学平衡常数为?K?=?____________; ?
②若保持温度不变,20?min?时再向容器中充入CO、N2各0.8?mol,平衡将________移动(填“向左”、?“向右”或“不”) ?
③20?min时,若改变反应条件,导致CO?浓度发生如图所示的变化,则改变的条件可能是__________(填序号); ?
a.缩小容器体积 ?b.增加CO2?的量 ? ?c.升高温度 ?d.加入催化剂
参考答案:(1)NH4Cl;3Cu+2NO3-+8H+?=?3Cu2++2NO↑+4H2O
(2)NH3?+?3Cl2?=?NCl3?+3HCl;Cl2
(3)①0.05?L・mol-1;②向左;③?bc
本题解析:
本题难度:一般
4、填空题 (13分) 如图所示,各物质间有下列转化关系:
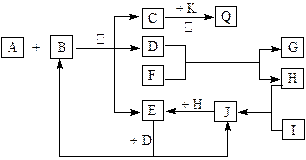
A、F分别为淡黄色固体,A与B的浓溶液反应可以生成C、D、E三种物质,D为无色液体,K为红色金属单质,能在加热条件下与C的浓溶液反应,生成气体Q。I和H为气态双原子分子。反应过程中部分条件和产物均略去。
(1)?I的电子式:____________________。
(2)?反应A + B的化学方程式:_________________________________________________。
(3)?将Q和E按2∶1同时通入品红溶液中,若产物之一含I,则现象可能为___________,原理是(用化学方程式表示)______________________________________________。
(4)?若标准状况下将11.2 L Q通入到500 mL 1.5 mol /L 的G溶液中,请将最终溶液的溶质成分及物质的量填入下表(可不填满)。?
溶质(化学式)
| 物质的量
|
?
| ?
|
?
| ?
|
?
| ?
参考答案:(13分) (1) 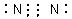 (2分) (2分)
(2) S + 6HNO3(浓) H2SO4 + 6NO2↑+ 3H2O(3分) H2SO4 + 6NO2↑+ 3H2O(3分)
(3) 无明显现象(1分)? 2NO2 + 4SO2 + 4H2O = N2 + 4H2SO4(3分)
(4) (4分,每空1分)
溶质(化学式)
物质的量
Na2SO3
0.25 mol
NaHCO3
0.25 mol
本题解析:略
本题难度:简单
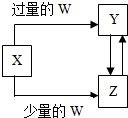
5、选择题 已知X、Y、Z、W均为中学化学中常见的单质或化合物,它们之间的转化关系如图所示(部分产物已略去).则W、X不可能是( )
| 选项 | W | X
A
盐酸
Na2CO3溶液
B
Cl2
Fe
C
CO2
Ca(OH)2溶液
D
NH3?H2O
AlCl3溶液
|
A.A
B.B
C.C
D.D
|
参考答案:BD
本题解析:
本题难度:简单