1、推断题 A、B、C、D是按原子序数由小到大排列的前20号元素的单质。B、E均为组成空气的成分。F的焰色反应呈黄色。在G中,非金属元素与金属元素的原子个数比为1∶2。在一定条件下,各物质之间的相互转化关系如下(部分产物未列出)
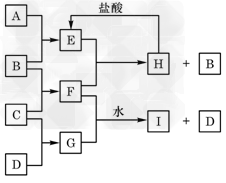
(1)A是___________,C是___________。
(2)H与盐酸反应生成E的化学方程式是_________________。
(3)E与F反应的化学方程式是_______________。
(4)F与G的水溶液反应生成I和D的离子方程式是_________________。
参考答案:(1)碳;钠?
(2)Na2CO3+2HCl=2NaCl+H2O+CO2↑
(3)2CO2+2Na2O2=2Na2CO3+O2
(4)Na2O2+S2-+2H2O=4OH-+S↓+2Na+
本题解析:
本题难度:一般
2、填空题 (10分)已知X为中学化学中一种常见的盐,F为淡黄色固体;M、N为常见的金属,N的氧化物可作耐火材料,可用它来制造耐火坩埚和耐高温试验仪器;H为气体单质,D为无色气体,D在空气中会出现红棕色,各物质的转化关系如下图,(部分反应产物已略去).
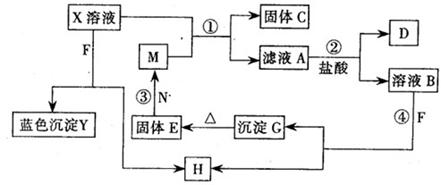
请回答下列问题;
(1)E的化学式为?
(2)将M丝插入盛有X溶液的试管中,反应一段时间后的现象是:?
(3)在反应①②③④中属于置换反应的是??(填序号).
(4)反应②的离子方程式为?
(5)用石墨作电极电解500mL X溶液,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成;电解一段时间后,取出A电极,洗涤、干燥、称量,电极增重1. 6g.请回答下列问题:
①写出电解时的阳极反应式??
②电解后溶液的pH为?假设电解前后溶液体积不变)
参考答案:(1)Fe2O3(1分)
(2)铁丝上附有红色物质,溶液颜色逐渐变为浅绿色(2分)
(3)①③(2分,每项1分,漏选一项扣1分,错选一项不得分)
(4) 3Fe2++NO3-? +4H+= 3Fe3+? +NO ↑? +2H2O(2分)
(5)? 4OH-=O2↑? +2H2O +4e-(或4OH- -4e- =O2↑+2H2O(2分)? 1(1分)
本题解析:略
本题难度:简单
3、推断题 物质A~G有下图所示转化关系(部分反应物、生成物没有列出)。其中A为某金属矿的主要成分,经过一系列反应可得到B和C。单质C可与E的浓溶液发生反应,G为砖红色沉淀。

请回答下列问题:
(1)写出下列物质的化学式:B________、E________、G?________;
(2)利用电解可提纯C物质,在该电解反应中阳极物质是________,阴极物质是______,电解质溶液是_____________;
(3)反应②的化学方程式是__________________________________;
(4)将0.23?mol?B和0.11?mol氧气放入容积为1L的密闭容器中,发生反应①,在一定温度下,反应达到平衡,得到0.12?mol?D,则反应的平衡常数K=________。若温度不变,再加入?0.50?mol氧气后重新达到平衡,则B的平衡浓度________(填“增大”、 “不变”或“减小”),氧气的转化率________(填“升高”、“不变”或“降低”),D的体积分数________(填“增大”、“不变”或“减小”)。
参考答案:(1)SO2;H2SO4;Cu2O
(2)粗铜;精铜;CuSO4溶液
(3)?Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
(4)?23.8L/mol;减小;降低;减小
本题解析:
本题难度:一般
4、推断题 根据下面物质间转换的框图,回答有关问题
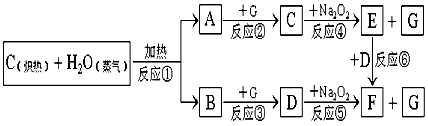
(1)写出框图中物质A、B、E、F分别指代物质的化学式:A._________B._________E._________
F._________
(2)如果2mol Na2O2与足量水蒸气反应,可得标准状况下气体的体积_________L;同时反应中转移电子总数是_________。(NA表示阿伏加德罗常数)
(3)如果A、B混合气体3.0g(平均摩尔质量15g・mol-1),在与G充分反应后,通过足量Na2O2层,可使Na2O2增重_________g,并得到O2_________mol。
参考答案:(1)H2;CO;NaOH;Na2CO3
(2)22.4L;2NA
(3)3.0g;0.1mol
本题解析:
本题难度:一般
5、填空题 A、B、C、D、E、F六种物质的相互转化关系如右图所示(反应条件及部分产物未列出)。
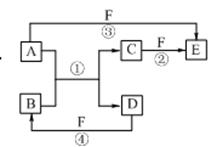
(1)若A是常见金属单质,与B的水溶液反应生成C和D。D、F是气体单质,D在F中燃烧时发出苍白色火焰。则F所对应的元素在周期表位置是?;反应②(在水溶液中进行)的离子方程式为?。
(2)若A、D为短周期元素组成的固体单质,A为金属,D为非金属。且③④两个反应都有红棕色气体生成,则反应①、④的化学方程式分别为
①??;④??。
(3)若A、D、F都是短周期非金属单质,且A、D所含元素同主族,A、F所含元素同周期,C是一种能与血红蛋白结合的有毒气体;则物质B的晶体类型是?,分子E的结构式是?。
参考答案:(1)第3周期第ⅦA族,2Fe2++Cl2=2Fe3++2Cl-
(2)①2Mg+CO2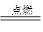 2MgO+C(条件不写得1分)
2MgO+C(条件不写得1分)
④C+4HNO3(浓)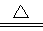 CO2↑+4NO2↑+2H2O(条件不写得1分)
CO2↑+4NO2↑+2H2O(条件不写得1分)
(3)原子晶体?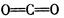
本题解析:(1)若A是常见的金属单质,反应①是置换反应,D、F是气态单质,根据框图可知,A与F生成E,C与F也能生成E,因此A只能为Fe,D为H2,F为Cl2,B为HCl,C为FeCl2,E为FeCl3。
(2)若A、D为短周期元素单质,且所含元素的原子序数A是D的2倍,所含元素的原子核外最外层电子数D是A的2倍,反应①是置换反应,根据框图可知,A为Mg,D为C,B为CO2,C为MgO,又知③和④两个反应中都有红棕色气体生成,F为HNO3。
(3)若A、D、F都是非金属单质,反应①是置换反应,A、D同主族,根据框图可知,A与F生成E,C与F也能生成E,因此只能是SiO2与C反应,则A是C、B是SiO2、C是CO、D是Si,E是CO2、F是O2。
本题难度:一般