1��ѡ���� ����˵����ȷ����
A��pH=7����Һһ����������Һ
B�����Է����еĻ�ѧ��Ӧ����һ���ǡ�H<0����S>0
C�����ȷ�Ӧ����������Ҫ���ϴ���������������ȷ�Ӧһ������Ҫ�����������
D��Ksp���������ܵ���ʵ����ʺ��¶��йأ���������Һ�е�����Ũ���й�
�ο��𰸣�B
���������A����ȷ����Ϊû��ָ���¶ȡ���Ӧ�Ƿ��ȷ�Ӧ�������ȷ�Ӧ���뷴Ӧ�����أ�C����ȷ��D����ȷ��Ksp�������ܵ���ʵ����ʺ��¶��йء����ݡ�G����H��T����S��֪��ѡ��B��ȷ����ѡB��
�����Ѷȣ�һ��
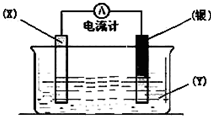
2������� ����������ԭ��Ӧ��2Ag+��aq��+Cu��s���TCu2+��aq��+2Ag��s����Ƶ�ԭ�����ͼ��ʾ����ش��������⣺
��1���缫X�IJ�����______���������ҺY��AgNO3���������缫������______���ʣ�
��2�����缫Ϊ��ص�______���������ĵ缫��ӦΪ______��X�缫�Ϸ����ĵ缫��ӦΪ______��
��3�����·�еĵ����Ǵ�______�缫����______�缫����ͭ������ѡ���
�ο��𰸣���1���ɷ�Ӧ��2Ag+��aq��+Cu��s���TCu2+��aq��+2Ag��s������֪���ڷ�Ӧ�У�Cu��������ʧ���ӣ�ӦΪԭ��صĸ�����Ag+�������ϵõ��ӱ���ԭ�������缫������Ag���ʣ�
�ʴ�Ϊ��Cu��Ag��
��2������Ϊ�����Խ�Cu����Ag��Ag+�������ϵõ��ӱ���ԭ���缫��ӦΪAg++e-=Ag����������ӦΪCu-2e-=Cu2+��
�ʴ�Ϊ������Ag++e-=Ag�� Cu-2e-=Cu2+��
��3��ԭ����У����ӴӸ��������·������������������Cu�������·����Ag�����ʴ�Ϊ��Cu��Ag��
���������
�����Ѷȣ�һ��
3������� ��12�֣���Zn����Cu���õ������Ӻ���ij�������Һ�У�����������ͼ��ʾװ�á��Իش��������⣺

��1�����������ҺΪϡ���ᣬ��Zn��Ϊԭ��ص� �����ɹ۲쵽Cu���������������� �����õ缫��Ӧʽ��ʾ������ ��
��2���������Ϊ����ͭ��Һ����Cu���Ϸ��� ��Ӧ��Zn���Ϸ�����Ӧ�ĵ缫��ӦʽΪ�� ��
��3�������������������У�Zn�����ٵ�������ȣ���Cu���ϣ�1���ͣ�2�����������ʵ�����֮��Ϊ�� ��
�ο��𰸣���1������(2��)����������(2��) 2H++2e-=H2+��(2��)
��2����ԭ (2��) Zn-2e-=Zn2+ (2��) ��3��1:32(3��)
�����������ԭ����нϻ��õĽ�����������ʧȥ���ӣ�����������Ӧ�����Ӿ����ߴ��ݵ������ϣ�������Һ�е��������������ƶ������������ƶ��������õ����ӣ�������ԭ��Ӧ��
��1��п��ͭ���ã�п�Ǹ�����ͭ����������Һ�е��������������õ����ӣ��缫��ӦʽΪ2H++2e-=H2+����
��2���������Ϊ����ͭ��Һ������Һ�е�ͭ�����������õ����ӣ�������ԭ��Ӧ������ͭ��п��Ȼ�Ǹ������缫��ӦʽΪ Zn-2e-=Zn2+��
��3��Zn�����ٵ�������ȣ�˵��ת�Ƶĵ�������ȵġ����Ը��ݵ��ӵ�ʧ�غ��֪���ɵ�������������ͭ�����ʵ�������ȵģ����Զ��ߵ�����֮����2:64��1:32��
�����Ѷȣ�һ��
4��ѡ���� ��M��N��P��Q�Ŀ����Ƭ����������ʵ�飺
��M��N�õ���������ͬʱ����ϡH2SO4�У�M��Ϊ����
��P��Q�õ���������ͬʱ����ϡH2SO4�У�������P�����ߡ�Q
��M��P������ͬʱ����ϡH2SO4��P��������������
��N��Q������ͬʱ����ϡH2SO4�У�Q������������Ӧ
�����ֽ����Ļ��˳��Ϊ
A��M>N>P>Q
B��M>P>Q>N
C��N>Q>P>M
D��P>M>N>Q
�ο��𰸣�B
���������ԭ��ع���ʱ����Ϊ���õĽ���Ϊ����������������Ӧ���ϲ����õĽ���Ϊ����������������ԭ���������������������������ʣ������ɸ��������������������Դ��жϽ����Ļ�����ǿ�������M��N�õ���������ͬʱ����ϡH2SO4�У�M��Ϊ�������������M��N����P��Q�õ���������ͬʱ����ϡH2SO4�У�������P�����ߡ�Q��PΪ�������������P��Q����M��P������ͬʱ����ϡH2SO4��P�������������ݣ�PΪ������������M��P����N��Q������ͬʱ����ϡH2SO4�У�Q������������Ӧ��QΪ������������Q��N��������Ļ�����˳��ΪM��P��Q��N����ѡB��
�����Ѷȣ���
5��ѡ���� �������ҺΪ����ͭ��ͭпԭ����У�ͭ�缫��
A������
B��������ԭ��Ӧ��һ��
C������
D�����������һ��
�ο��𰸣�BCD
���������ͭпԭ����У�п��ͭ���ã���пΪ����������ʧ���ӵ�������Ӧ��
��ͭΪ�����������õ��ӵĻ�ԭ��Ӧ����ѡB��C��D��
�����Ѷȣ�һ��