1��ѡ���� ���е��뷽��ʽ�У���ȷ����
A.Al2��SO4��3=2Al+3+3SO4-2
B.CuCl2=Cu2++2Cl-
C.K2SO4=2K++S6++4O2-
D.Na2CO3=Na++CO
�ο��𰸣�B
���������������A����������ǿ�������Һ����ȫ�����������ӣ���ע����������ɴ���
B���Ȼ�ͭ������ˮ��ǿ�������ȫ��������ͭ���Ӻ������ӣ�
C���������Һ�е���������������Ӻͼ����ӣ�
D��̼������Һ�е������������Ӻ�̼������ӣ�ע�����غ㣮
���A����������ǿ�������Һ����ȫ���룬���뷽��ʽΪ��Al2��SO4��3=2Al3++3SO42-����A����
B���Ȼ�ͭ������ˮ��ǿ�������ȫ��������ͭ���Ӻ������ӣ����뷽��ʽΪ��CuCl2=Cu2++2Cl-����B��ȷ��
C���������Һ�е���������������Ӻͼ����ӣ����뷽��ʽΪ��K2SO4=2K++SO42-����C����
D��̼������Һ�е������������Ӻ�̼������ӣ����뷽��ʽΪ��Na2CO3=2Na++CO32-����D����
��ѡB��
���������⿼���˵��뷽��ʽ�������жϺ���д������ע�������ܽ��Է��������ӷ�����д�������������ӵ��жϣ���Ŀ�ϼ�
�����Ѷȣ�����
2��ѡ���� ��������ĵ���ƽ�ⳣ�����±���
����
| HCOOH
| HCN
| H2CO3
|
����ƽ�ⳣ��(25��)
| Ki��1.77��10��4
| Ki��4.9��10��10
| Ki1��4.3��10��7
Ki2��5.6��10��11
|
����ѡ�������ǣ� ��
��2CN����H2O��CO2=2HCN��CO32-
��2HCOOH��CO32-=2HCOO����H2O��CO2��
���к͵��������pH��HCOOH��HCN������NaOH����ǰ��С�ں���
�ܵ��������Ũ�ȵ�HCOONa��NaCN��Һ��������������ǰ��С�ں���
A.�٢� B.�ڢ� C.�ۢ� D.�٢�
�ο��𰸣�D
������������ݵ��볣����֪����HCOOH��H2CO3��HCN��HCO3-��A����B��ȷ�����������pH��HCOOH��HCN��Һ��������HCN��Һ���࣬���к�ʱ���ĵ�NaOH�����࣬C��ȷ�����ݵ���غ㣬n(HCOO��)��n(OH��)��n(Na��)��n(H��)��n(CN��)��n(OH��)��n(Na��)��n(H��)��������������n(Na��)��n(H��)��2������NaCN��ˮ��̶ȴ�NaCN��Һ�е�n(OH��)��n(H��)С��D����
�����Ѷȣ�һ��
3������� ��8�֣�
I.��֪��25��ʱ��HF��HCN��H2CO3�ĵĵ���ƽ�ⳣ�������ʾ��
��1��д��̼��ĵ�һ������ƽ�ⳣ������ʽ��K1= ��
��2������Na2CO3��Һ�м�������HF��Һ��������Ӧ�����ӷ���ʽ��
����NaCN��Һ��ͨ������CO2��������Ӧ�����ӷ���ʽ��
II. �õ�ⷨ��ȡ����þʱ����Ҫ��ˮ�Ȼ�þ���ڸ����HCl�����м���MgCl2��6H2Oʱ���ܵõ���ˮMgCl2����ԭ���� ��
�ο��𰸣���I. ��1��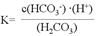 ��2�֣�
��2�֣�
��2����2HF+CO32-=2F-+H2O+CO2�� ��2�֣���CN-+H2O+CO2= HCN+HCO3- ��2�֣�
II. �ڸ����HCl�����У�������MgCl2��ˮ�⣬�Ҵ�����MgCl2��6H2O���Ȳ�����ˮ��������2�֣�
�����������1��̼���Ƕ�Ԫ���ᣬ�ֱ���룬̼��ĵ�һ������ƽ�ⳣ������ʽ��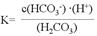 ����2������������HF>H2CO3��������Na2CO3��Һ�м�������HF��Һ��������Ӧ�����ӷ���ʽ2HF+CO32-=2F-+H2O+CO2�������������ԣ�H2CO3> HCN> HCO3- ,��NaCN��Һ��ͨ������CO2��������Ӧ�����ӷ���ʽ��CN-+H2O+CO2= HCN+HCO3-��II. �õ�ⷨ��ȡ����þʱ����Ҫ��ˮ�Ȼ�þ���ڸ����HCl�����м���MgCl2��6H2Oʱ���ܵõ���ˮMgCl2����ԭ�����ڸ����HCl�����У�������MgCl2��ˮ�⣬�Ҵ�����MgCl2��6H2O���Ȳ�����ˮ�������Ӷ��õ���ˮMgCl2��
����2������������HF>H2CO3��������Na2CO3��Һ�м�������HF��Һ��������Ӧ�����ӷ���ʽ2HF+CO32-=2F-+H2O+CO2�������������ԣ�H2CO3> HCN> HCO3- ,��NaCN��Һ��ͨ������CO2��������Ӧ�����ӷ���ʽ��CN-+H2O+CO2= HCN+HCO3-��II. �õ�ⷨ��ȡ����þʱ����Ҫ��ˮ�Ȼ�þ���ڸ����HCl�����м���MgCl2��6H2Oʱ���ܵõ���ˮMgCl2����ԭ�����ڸ����HCl�����У�������MgCl2��ˮ�⣬�Ҵ�����MgCl2��6H2O���Ȳ�����ˮ�������Ӷ��õ���ˮMgCl2��
���㣺��������ĵ���ƽ�ⳣ����Ӧ�á����ӷ���ʽ����д���ε�ˮ���������ȡ������Ӱ���֪ʶ��
�����Ѷȣ�һ��
4������� ij��Ԫ��H2A���뷽��ʽ�ǣ�H2A=H++HA-��HA-?A2-+H+���ش��������⣺
��1��Na2A��Һ��______�ԣ������ǣ������ӷ���ʽ��ʾ��______��
��2����0.1mol/LNaHA��Һ��pH=2����0.1mol/LH2A��Һ�������ӵ����ʵ���Ũ�ȿ���______0.11mol/L�����������������=����������______��
��3��ij�¶��£���10mL��0.1mol/LNaHA��Һ�м���0.1mol/LKOH��ҺVmL�����ԣ���ʱ��Һ�����¹�ϵһ����ȷ����______����д��ĸ����
A����ҺpH=7 B��ˮ�����ӻ�KW=c2��OH-��
C��V=10D��c��K+����c��Na+��
��4��0.1mol/LNaHA��Һ�и�����Ũ���ɴ�С��˳����______��
�ο��𰸣���1������H2A�ĵ����Ƿֲ��������֪��H2A�����ᣬ����Na2A��Һ�Լ��ԣ�ˮ��ԭ���ǣ�H2O+A2-?HA-+OH-���ʴ�Ϊ�����ԣ�H2O+A2-?HA-+OH-��
��2��0.1mol?L-1H2A��Һ��H2A�TH++HA-�������0.1mol/LH+��0.1mol?L-1NaHA��Һ��pH=2������HA-?H++A2-��֪�������0.01mol/LH+������һ���������ɵ�H+������HA-�ĵ��룬������Һ�������ӵ����ʵ���Ũ��С��0.1mol/L+0.01mol/L��
�ʴ�Ϊ������H2A��һ���������ɵ�H+������HA-�ĵ��룻
��3��A�������¶Ȳ�֪����������ʱ��ҺpH����ȷ������A����
B������c��OH-��=c��H+����Kw=c��OH-��c��H+��=KW=c2��OH-������B��ȷ��
C��HA-�� OH-ǡ�÷�Ӧʱ����A2-����Һ�ʼ��ԣ���֪��ҺΪ���ԣ�˵��NaHA��Һ��ʣ�࣬��V��10����C����
D������Cѡ���жϣ�NaHA����������c��K+����c��Na+������D��ȷ��
�ʴ�Ϊ��BD��
��4��NaHA��Һ�����ԣ�����HA-?H++A2-����c��Na+����c��HA-����c��H+����c��OH-�������ˮ�ĵ���H2O?H++OH-��ͬʱ�в���A2-����ˮ�⣬ʹc��A2-����С������c��H+����c��A2-������NaHA��Һ�и�������Ũ���ɴ�С��˳��Ϊc��Na+����c��HA-����c��H+����c��A2-����c��OH-�����ʴ�Ϊ��c��Na+����c��HA-����c��H+����c��A2-����c��OH-����
���������
�����Ѷȣ�һ��
5������� ������SOCl2��һ��Һ̬������е�Ϊ77�档��ʢ10mlˮ����ƿ��С�ĵμ�8��10��SOCl2�ɹ۲쵽���ҷ�Ӧ��Һ�����γɰ��������д̼�����ζ������ų����������ʹʪ���Ʒ����ֽ��ɫ���ڷ�Ӧ�����Һ�еμ�AgNO3��Һ��������һ�ֲ�����ϡHNO3�İ�ɫ������
��1���Ծ�����ʵ����ʵ��д��SOCl2��ˮ��Ӧ�Ļ�ѧ����ʽ ��
��2����ZnCl2��Һ�������ɣ��ò�����ˮZnCl2����ҵ�ϳ���ZnCl2?2H2O��SOCl2������ȡZnCl2���Խ�����ӷ���ʽ����ԭ�� ��
��3����ѧ�Ҿ������� ˮ��ԭ���Ʊ����ײ��ϣ���д����TiCl4�Ʊ�TiO2��xH2O�Ļ�ѧ����ʽ�� ��
ˮ��ԭ���Ʊ����ײ��ϣ���д����TiCl4�Ʊ�TiO2��xH2O�Ļ�ѧ����ʽ�� ��
�ο��𰸣�
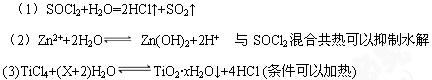
�����������
�����Ѷȣ�����