| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点总结《盐类水解的原理》考点巩固(2017年最新版)(十)
参考答案: 本题解析: 本题难度:一般 3、填空题 (6分) |
参考答案:(1)A (2)酸 Al3+ +3H2O Al(OH)3+3H+ Al2O3
Al(OH)3+3H+ Al2O3
本题解析:①热纯碱溶液洗涤油污的能力比冷纯碱溶液强是因为纯碱是强碱弱酸盐,水解使溶液显碱性。而盐的水解反应是吸热反应,所以升高温度促进盐的水解,因此去污能力强。与沉淀溶解平衡无关,错误;②误将钡盐[BaCl2、Ba(NO3)2]当作食盐食用时,若服用0.5%的Na2SO4溶液,就会发生沉淀反应产生BaSO4沉淀,降低了人体内的Ba2+的浓度,从而达到解毒的目的,这与沉淀溶解平衡有关,正确;③当水中含有CO2等酸性气体时就会发生反应产生容易溶解于水碳酸氢盐,随水分而流失,从而促进了盐的溶解和电离,盐再溶解,最后逐步形成石灰岩(喀斯特地貌)的溶洞;这与沉淀溶解平衡有关,正确;⑤使用泡沫灭火器时是盐的双水解反应相互促进,产生更多的Al(OH)3,在CO2的气体压力作用下以泡沫的形式出现,“泡沫”生成的原理与沉淀溶解平衡无关,错误。故正确的说法是②③④,故选项是A。(2)氯化铝是强酸弱碱盐,若碱根离子水解消耗水电离产生的OH-,最终当溶液处于平衡时, c(H+)>c(OH-),所以溶液呈酸性;水解的离子方程式表示为Al3+ +3H2O Al(OH)3+3H+ 。水解产生的HCl会随着水分的蒸发而挥发,所以蒸干得到的固体是Al(OH)3,若再灼烧,则Al(OH)3发生分解反应产生Al2O3和水,所以最后得到的主要固体产物是Al2O3。
Al(OH)3+3H+ 。水解产生的HCl会随着水分的蒸发而挥发,所以蒸干得到的固体是Al(OH)3,若再灼烧,则Al(OH)3发生分解反应产生Al2O3和水,所以最后得到的主要固体产物是Al2O3。
考点:考查盐的水解平衡、沉淀溶解平衡及盐水解的应用的知识。
本题难度:一般
4、填空题 下表中列出五种短周期元素A、B、C、D、E的信息,请推断后回答:
| 元素 | 有 关 信 息 |
| A | 元素主要化合价为-2,原子半径为0.074 nm |
| B | 所在主族序数与所在周期序数之差为4 |
| C | 原子半径为0.102 nm,其单质为黄色晶体,可在A的单质中燃烧 |
| D | 最高价氧化物的水化物能按1 |
参考答案:
本题解析:
本题难度:困难
5、简答题 I、(1)NaHCO3是一种______(填“强”或“弱”)电解质;
(2)写出HCO3-水解的离子方程式:______;
(3)常温下,0.1mol?L-1NaHCO3溶液的pH大于8,则溶液中Na+、HCO3-、H2CO3、CO32-、OH-五种微粒的浓度由大到小的顺序为:______.
Ⅱ、醋酸是一种弱电解质.某温度下,相同pH值的盐酸和醋酸溶液分别加水稀释,平衡pH值随溶液体积变化的曲线如图所示.则图______(填“I”或“Ⅱ”)为醋酸稀释的图象.
Ⅲ、Ba(OH)2是一种强电解质,现有25℃、pH=13的Ba(OH)2溶液.
(1)溶液中由水电离出c(OH-)=______;
(2)与某浓度盐酸溶液按体积比(碱与酸之比)1:9混合后,所得溶液pH=11(假设混合溶液的体积等于混合前两溶液的体积和),该盐酸溶液的pH=______.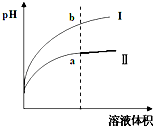
参考答案:Ⅰ、(1)NaHCO3属于盐,在水溶液中完全电离,属于强电解质,故答案为:强;
(2)HCO3-水解生成碳酸与氢氧根离子,水解离子方程式为HCO3-+H2O?H2CO3+OH-,
故答案为:HCO3-+H2O?H2CO3+OH-;
(3)常温下,0.1mol?L-1NaHCO3溶液的pH大于8,c(OH-)>c(H+),说明HCO3-水解程度大于其电离程度,故c(Na+)>c(HCO3-)、c(H2CO3)>c(CO32-),水解程度不大所以c(HCO3-)>c(H2CO3)、c(HCO3-)>c(OH-),溶液中氢氧根来源于水的电离与HCO3-水解,故c(OH-)>c(H2CO3),所以c(Na+)>c(HCO3-)>c(OH-)>c(H2CO3)>c(CO32-),
故答案为:c(Na+)>c(HCO3-)>c(OH-)>c(H2CO3)>c(CO32-);
Ⅱ、盐酸是强电解质,醋酸是弱电解质,相同pH值的盐酸和醋酸溶液分别加水稀释,醋酸稀释促进醋酸电离继续产生氢离子,故稀释相同的倍数,醋酸的PH增大的较小,故图Ⅱ为醋酸稀释的图象,
故答案为:Ⅱ.
Ⅲ、(1)pH=13的Ba(OH)2溶液中氢离子使由水电离产生的,水电离产生的c(H+)等于溶液中水电离出c(OH-),故水电离出c(OH-)=c(H+)=10-13mol/L,
故答案为:10-13mol/L;
(2)pH=13的Ba(OH)2溶液中c(OH-)=0.1mol/L,与某浓度盐酸溶液按体积比(碱与酸之比)1:9混合后,假定体积分别为1L、9L,所得溶液pH=11,即混合后溶液中c(OH-)=10-3mol/L,令盐酸的浓度为amol/L,则混合后溶液中n(OH-)=1L×0.1mol/L-9L×amol/L=10-3mol/L×(1L+9L),解得a=0.01,所以pH=2
故答案为:2;
本题解析:
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点整理《物质的分离.. | |