1、选择题 用NA表示阿佛加德罗常数,下列叙述正确的是
A.电解AgNO3溶液析出10.8克银需0.1NA个电子
B.通常情况5.6升氢气含0.5NA个原子
C.9克水含质子数为4NA
D.2NA个硫酸分子与19.6克磷酸含相同的氧原子数
参考答案:A
本题解析:A:由电极反应Ag--e-=Ag可求得析出10.8克银时转移0.1NA个电子,正确
B:非标准状况,不能计算出氢气的量
C:9克水H2O 含质子数为: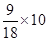 NA,即5NA
NA,即5NA
D:前者含有8NA个氧原子,后者H3PO4含有: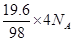 =0.8NA个氧原子
=0.8NA个氧原子
故答案为A
本题难度:一般
2、选择题 同温同压下气体A2和气体B2等体积完全化合生成气体AXBY,反应前后体积不变,则X?和Y?的值是( )
A.X=1Y=1
B.X=1Y=2
C.X=2Y=1
D.X=2Y=2
参考答案:相同温度和压强下,气体的体积之比等于物质的量之比,等于化学反应方程式的系数之比,反应前后体积不变,所以1体积的A2气体与1体积的B2气体化合生成2体积的气态化合物AXBY,反应方程式可以表示为:A2+B2=2AXBY,根据原子守恒,所以X=1,Y=1.
故选:A.
本题解析:
本题难度:简单
3、选择题 某固态非金属单质A和氧气发生化合反应生成B(B为气体),在同温同压的条件下,气体B的体积是反应掉氧气体积的两倍.以下对B的分子组成的推测一定正确的是( )
A.有1个氧原子
B.有2个氧原子
C.有1个A原子
D.有2个A原子
参考答案:同温同压下气体的Vm相同,由n=VVm可知,气体的体积之比等于物质的量之比,则有1molO2可生成2molB,
则B中应含有1个O,
故选A.
本题解析:
本题难度:一般
4、选择题 设NA为阿伏加德罗常数的值,下列有关其说法正确的是
A.物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl-个数为NA
B.标准状况下,22.4LH2O含有的分子数为NA
C.在室温和常压下,71 g Cl2含有2NA个Cl原子
D.在同温、同压下,相同体积的任何气体,所含分子数和原子数相同
参考答案:C
本题解析:A选项没有给出溶液的体积,故无法计算Cl-的个数;B选项中,标准状态下水的密度为1g/cm3,故水分子的分子数为22.4L×1×103g/L÷18g/mol≈1.24×103mol;C选项中,n(Cl2)=m/M=71g÷71g/mol=1mol,故n(Cl)=2mol;根据阿伏伽德罗定律可知,同温、同压下,相同体积的任何气体都含有相同数目的粒子,如N2和NH3,其所含分子数相同,但是原子数明显不同。
点评:化学计量是学习化学的基础,考生应熟练掌握。高考的考查主要为阿伏伽德罗常数的相关知识点。
本题难度:简单
5、填空题 下列分子数由少至多的顺序是______,质量由小到大的顺序______.
①6g氢气?②2mol氨气?③4℃时?9mL水④1.204×1023个硫酸分子?⑤标准状况下5.6LCO2.
参考答案:①6g氢气,分子数N=nNA=mM×NA=6g2g/mol×NA=3NA,质量是6g.
②2mol氨气,分子数N=nNA =2NA,m=nM=2mol×17g/mol=34g.
③4℃时?9mL水,其质量是9g.分子数N=nM×NA=9g18g/mol×NA=0.5N A
④1.204×1023个硫酸分子,分子数N=0.2NA,质量m=NNA×M=0.2NANA×98g/mol=19.6g
⑤标准状况下5.6LCO2,,分子数N=VVm×NA=5.6L22.4L/mol×NA=0.25NA,m=VVm×M=5.6L22.4L/mol×44g/mol=11g
故答案为:④⑤③②①;①③⑤④②
本题解析:
本题难度:一般