1、填空题 有一包白色粉末,可能由KCl、BaCO3、BaCl2、KNO3、NH4NO3和Na2SO4中的一种或几种组成。现进行下列实验:
(1)将此粉末溶于水中,得到无色透明溶液A及白色沉淀B,过滤。
(2)取沉淀物B,加稀HNO3后,沉淀物B不溶解。
(3)取少量溶液A,加入适量的NaOH溶液,加热,产生无色有刺激性气味并能使湿润的红色石蕊试纸变蓝色的气体。
(4)再取少量溶液A,滴入AgNO3溶液,充分反应后,有白色沉淀生成,该沉淀不溶于稀硝酸。
据此推断,该白色粉末中,一定含有?,肯定不含有?,可能含有?。
参考答案:一定含有:BaCl2、Na2SO4、NH4NO3 ;肯定不含有:BaCO3 ;可能含有:KCl、KNO3
本题解析:略
本题难度:简单
2、填空题 氯化铵简称“氯铵”,又称卤砂,为无色晶体或白色结晶性粉末,易溶于水中,在工农业生产中用途广泛。以氯化钠和硫酸铵为原料制备氯化铵及副产品硫酸钠,工艺流程如下:
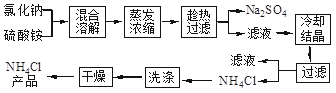
氯化铵和硫酸钠的溶解度随温度变化如图所示。回答下列问题:
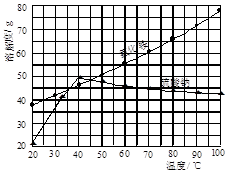
(1)实验室进行蒸发浓缩用到的主要仪器有?、烧杯、玻璃棒、酒精灯等。
(2)实验过程中趁热过滤的目的是?。
(3)写出“蒸发浓缩”时发生的化学方程式:??。
(4)某研究性学习小组为测定该NH4Cl产品中氮的含量,设计了如图装置,并进行了讨论。

甲同学:根据此实验测得的数据,计算的NH4Cl产品的含氮量可能偏高,因为实验装置中存在一个明显缺陷是:? ____?。
乙同学:实验过程中,往烧瓶中加入的浓氢氧化钠溶液的离子反应方程式为?,反应过程中NaOH一定要足量并充分加热,原因是?。
用改进后的实验装置重新进行实验,称取13.0gNH4Cl产品,测得实验后B装置增重3.4g。则该化肥含氮量为?。
参考答案:(1)蒸发皿
(2)防止氯化铵晶体析出而损耗
(3)(NH4)2SO4+2NaCl= Na2SO4↓+2NH4Cl
(4)①A、B装置间缺一个干燥装置?② NH4++OH- NH3↑+H2O
NH3↑+H2O
使氯化铵充分反应完全转化为NH3? 21.5%
本题解析:(1)实验室进行蒸发浓缩用到的主要仪器有蒸发皿、烧杯、玻璃棒、酒精灯等,
(2)由图像可以看出,在某一温度范围内,氯化铵的溶解度低于硫酸铵的溶解度,所以趁热过滤防止氯化铵晶体析出而损耗,可以使硫酸铵以沉淀形式滤出而氯化铵留在滤液里。
(3)蒸发浓缩时硫酸铵以固体形式存在,所以化学方程式为(NH4)2SO4+2NaCl= Na2SO4↓+2NH4Cl
△
高温
?(4)①氨气在进入B之前未干燥,所以含氮量偏高,应在A、B装置间加一个干燥装置,②烧瓶中发生的离子方程式是强碱与铵盐溶液的反应,离子方程式为NH4++OH-= NH3↑+H2O;碱要足量的目的就是使铵根离子全部转化为氨气;3.4g即为氨气的质量,其氮元素的质量为3.4g×14÷17=2.8g,所以含氮量为2.8g/13.0g×100%=21.5%。
本题难度:困难
3、简答题 海洋约占地球表面积的71%,海水中化学资源的利用具有非常广阔的前景.
(1)目前世界上60%的镁是从海水中提取的,其主要步骤如图所示:
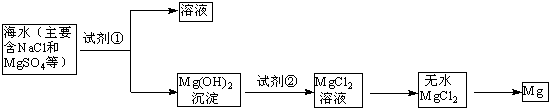
①试剂①宜选用石灰乳且必须过量,过量的目的是______.
②镁蒸气宜在______(填序号)气体冷却后得到镁锭(A.N2B.CO2C.ArD.空气)
(2)工业以浓缩海水为原料提取溴的部分过程如图:

某课外小组在实验室模拟上述过程设计如图所示装置进行实验(所有橡胶制品均已被保护,夹持装置已略去):
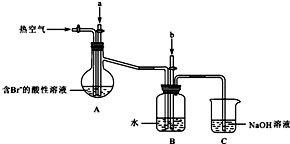
③A装置中通入a气体时,反应的离子方程式表示为:______.
④A装置中通入a气体一段时间后,停止通入,改通热空气.通入热空气的目的是:______.
⑤反应过程中,B装置中产生的两种主要阴离子为______.
⑥C装置的作用是______.
参考答案:(1)①过量的石灰乳能使Mg2+完全转化为Mg(OH)2沉淀,故答案为:使Mg2+完全转化为Mg(OH)2沉淀;
②镁是活泼的金属,能和氧气、氮气以及CO2反应,所以应该在Ar中冷却,故答案为:C;
(2)③a气体应该是氯气,能把溴离子氧化生成单质溴,反应的离子方程式是Cl2 +2Br-=2Cl-+Br2,故答案为:Cl2+2Br-=2Cl-+Br2;
④通入热空气能将溴从蒸馏烧瓶A中吹出,提高产量,故答案为:将溴从蒸馏烧瓶A中吹出;
⑤b气体是SO2,溴水能把SO2氧化生成溴化氢和硫酸,所以B装置中产生的两种主要阴离子为SO42-、Br-,故答案为:SO42-、Br-;
⑥氢氧化钠能吸收未反应完的Cl2、Br2、SO2等有毒气体,防止污染空气,故答案为:吸收未反应完的Cl2、Br2、SO2等有毒气体,防止污染空气.
本题解析:
本题难度:一般
4、选择题 下列有关实验的叙述正确的是 ( ?)
A.用HF溶液可以除去硅晶体中含有的少量二氧化硅晶体
B.向两份Fe3O4固体中分别加入HCl溶液与HI溶液,二者反应现象一样
C.向某溶液中滴加NaOH溶液后又加入酚酞,溶液呈红色,说明原溶液中含有NH4+
D.向某溶液中加入足量的稀HNO3溶液,所得气体能使澄清石灰水变浑浊,证明该溶液中存在CO32-或HCO3-
参考答案:D
本题解析:A.Si+4HF=SiF4↑+2H2↑;SiO2+4HF=SiF4↑+2H2O.二者均被反应消耗掉。错误。B发生的反应为:Fe3O4+8HCl=2FeCl3+FeCl2+4H2O ; Fe3O4+8HI= 3FeCl2+4H2O+I2.前者是复分解反应,后者是氧化还原反应。现象并不相同。错误。C.由于向溶液中加入了NaOH溶液,所以再滴加酚酞试液是溶液由于含有碱性溶液而呈红色,这不能确定是否含有NH4+。错误。D因为HNO3溶液有强的氧化性,可以把SO32-或HSO3-氧化为SO42-。所以向某溶液中加入足量的稀HNO3溶液,所得气体就排除了SO2的可能性。能使澄清石灰水变浑浊,就可以证明该溶液中存在CO32-或HCO3-。正确。2、Fe3O4的化学性质及CO32-或HCO3-等离子的检验的知识。
本题难度:一般
5、填空题 某氯化钠样品中含有少量的硫酸钠和碳酸钠杂质,按下列流程进行净化,回答下列问题。
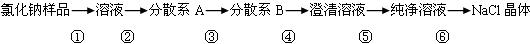
(1)分散系A、B都属于?(选填“溶液”“胶体”或“浊液”)。
(2)写出以下步骤所需的试剂(用化学式表示)
②??③??⑤??
(3)写出以下步骤的实验操作名称①??④??⑥??
(4)第④步中要用到的玻璃仪器有烧杯、?、?
(5)写出第②步有关反应的离子方程式
?
参考答案:(1)?浊液?(2)试剂②? BaCl2?③ Na2CO3?⑤ HCl??
(3)操作①?溶解??④?过滤??⑥?蒸发结晶??
(4)搅拌、引流?(5) Ba2+ +CO32-= BaCO3↓、?Ba2+ +SO42-= BaSO4↓
本题解析:略
本题难度:简单