1��ѡ���� ���л����Һ�У�������Ũ�ȵĴ�С˳����ȷ����
[? ]
A��10mL0��1mol/L��ˮ��10mL0��1mol/L�����ϣ�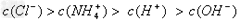
B��10mL1mol/LNH4Cl��Һ��5mL2mol/LNaOH��Һ��ϣ�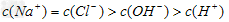
C��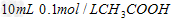 ��Һ��
��Һ��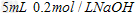 ��Һ��ϣ�
��Һ��ϣ�
?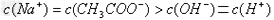
D����pH=3��������pH=11�İ�ˮ�������Ϻ�c��NH4+����c��Cl-����c��OH-����c��H+��
�ο��𰸣�C
���������
�����Ѷȣ�һ��
2��ѡ���� ����ʱ����CH3COOH��Һ��NaOH��Һ�������Ϻ���Һ�����ԣ������и�����ȷ���ǣ�������
A�����ǰ��c��CH3COOH����c��NaOH��
B�����ǰ��pH��CH3COOH��+pH��NaOH��=14
C����Ϻ�c��Na+���Tc��CH3COO-��
D����Ϻ�c��Na+����c��CH3COO-����c��OH-����c��H+��
�ο��𰸣�A������Ϊ���ᣬ��c��CH3COOH��=c��NaOH��������ǡ�÷�Ӧ����Һ�ʼ��ԣ���Һ�����ԣ�����Ӧ�����������ǰ��c��CH3COOH����c��NaOH������A��ȷ��
B����pH��CH3COOH��+pH��NaOH��=14��Ӧ��c��OH-��=c��H+�������ڴ���Ϊ���ᣬ����̶Ƚ�С�����ߵ������Ϻ�������϶࣬��Һ�����ԣ���B����
C����Һ�����ԣ���Ӧ����c��OH-��=c��H+��������c��Na+��+c��H+��=c��CH3COO-��+c��OH-������֪c��Na+���Tc��CH3COO-������C��ȷ��
D����Һ�����ԣ�Ӧ����c��Na+��=c��CH3COO-���� c��OH-��=c��H+������D����
��ѡAC��
���������
�����Ѷȣ���
3������� ��Ҫ��ش���������
(1)KHSO4��Һ��________�ԣ���ᡱ?���?�����ԡ�������ԭ���ǣ��õ��뷽��ʽ��ʾ��_________________��
(2)?KHCO3��Һ��________�ԣ���ᡱ?���?�����ԡ�������ԭ���ǣ������ӷ���ʽ��ʾ��____________________��?
(3)?����������Һ��ϣ����ӷ�Ӧ����ʽΪ___________________��
(4)��Na2CO3��Һ�е����̪����Һ��졣���ڸ���Һ���ٵ��������BaCl2��Һ�����۲쵽��������________________����ԭ����(�����ӷ���ʽ�ͼ�Ҫ����˵��)?____________________________________________��
�ο��𰸣���1���KHSO4=K++H++SO42-
��2���HCO3- + H2O  H2CO3 + OH-
H2CO3 + OH-
��3��HCO3- +H+ =CO2�� +H2O
 ��4����Һ��ɫ���dz��Ba2+ + CO32- =BaCO3�� ��
��4����Һ��ɫ���dz��Ba2+ + CO32- =BaCO3�� �� ��
�� ����BaCO3��ʹ��Һˮ����Լ���
����BaCO3��ʹ��Һˮ����Լ���
���������
�����Ѷȣ�һ��
4��ѡ���� �����£������������������Һ��ϣ�������Һ?pH=7�������Һ�У�������
A��[HCOO-]��[Na+]
B��[HCOO-]��[Na+]
C��[HCOO-]=[Na+]
D����ȷ��[HCOO-]��[Na+]�Ĺ�ϵ
�ο��𰸣�C
���������
�����Ѷȣ���
5��ѡ���� ��֪���ԣ�HCOOH>CH3COOH>C6H5OH���ж���ͬ���ʵ���Ũ�ȵ�������Һ�ļ�����������
[? ]
A. C6H5ONa
B. CH3COONa
C. HCOONa
D. NaOH��Һ
�ο��𰸣�C
���������
�����Ѷȣ�һ��