1������� ��14�֣���I����A��B��C��D��E��F�������ʵ����Ԫ�ؾ�Ϊ������Ԫ�أ����ǵ�ת����ϵ��ͼ�����з�Ӧ��Ϊ�û���Ӧ��
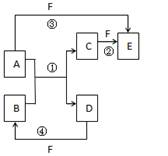
��1����A��D��FΪ�ǽ������ʣ���A��Dͬ���壬A��Fͬ���ڣ���F��??����Ӧ�ٵĻ�ѧ����ʽΪ??��
��2������B��C��F������̬���ʣ���B�ж����ۡ��ܷ�Ӧ�ж���ˮ���ɣ���Ӧ�����ڷŵ������½��У�д����Ӧ�ٵĻ�ѧ����ʽΪ??����Ӧ��Ϊ?�ȷ�Ӧ
��3����A��DΪ���ʣ�������Ԫ�ص�ԭ������A��D��������ԭ�ӵ�����������D��A������, F��D����Ԫ�ص�����������ˮ�����Ӧ�ٵ�ʵ�������ǣ�
��Ӧ�ܵĻ�ѧ����ʽΪ??��FΪŨ��Һ��
��II��X��Y��Z��W 4��Ԫ�ء���֪����X+��Y-�������Ӿ�����ͬ�ĵ��Ӳ�ṹ����ZԪ��ԭ�Ӻ�����������YԪ��ԭ�Ӻ�����������9������Y��Z��Ԫ�ؿ����γ��ĺ�41�����ӵĸ�һ�������ӣ���WԪ��ԭ��������Ӳ��ϵĵ�����ռ���������������֮�����ݴ���գ� YԪ����?��ZԪ����?����W��Z��Ԫ�����γɵĺ�22�����ӵĻ�����A�Ľṹʽ��?����X��Y��Z��Ԫ�ذ�ԭ�Ӹ�����Ϊ1��1��1�γɵĻ�����B�ĵ���ʽ��?��
�ο��𰸣���14�֣���I��O2?�� 1�֣�? SiO2�� 2C?��SiO2?��2CO�� 2�֣�
2NH3�� 3Cl2?�� N2��6HCl?�� 2�֣����ȣ� 1�֣�?þ��ȼ�գ������⣬���ɺڰ����ֹ��壨 2�֣�? C ��4HNO3��Ũ��?��CO2����4NO2����2H2O �� 2�֣��������ԣ�
��II��Cl�� 1�֣���O�� 1�֣�? ,O=C=O�� 1�֣� ,K+���UO�UCl�U��-�� 2�֣�
�����������1��ͬ�����ķǽ������ʵ��û���Ӧ�����������ֻ��SiO2��C�ķ�Ӧ��
��2��ͻ�ƿ����ڷ�Ӧ�����ڷŵ�������½��У���ΪN2��O2�ŵ練Ӧ����NO���塣��BΪ�ж����嵥�ʣ�ͨ��ΪCL2������֪��Ӧ��Ϊ��ҵ�ϼ�������Ƿ�й©�ķ�������Ӧ����Ϊ���Ĵ����������ڷ��ȷ�Ӧ��
��3������A��DΪ���ʣ�������Ԫ�ص�ԭ������A��D�����������û���ӦΪMg��CO2����ķ�Ӧ��
��II��X��Y��Z��W 4��Ԫ�ض�Ӧ��Ԫ�ط���Ϊ��K��CL��O��C��
�����Ѷȣ���
2������� ������ͼ����֮���ת����ϵ���ش�
��1��д��A��B��C�Ļ�ѧʽ��A______��B______��C______��
��2��д�����и����Ļ�ѧ��Ӧ����ʽ��
A��B��______��
A��Cu��______��
�ο��𰸣�AFe
���������
�����Ѷȣ�һ��
3������� ͼ��A��J�ֱ����һ�ַ�Ӧ����������֪A���ȷֽ�õ������ʵ�����B��C��D��̬���ʣ�ͼ�в���������δ�г�
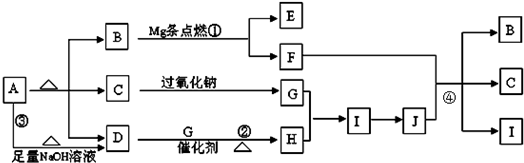
��ش�
��1��B�Ľṹʽ______��D���ӵĿռ乹��Ϊ______��
��2��д����Ӧ�١��ܵĻ�ѧ����ʽ
? ? ?��______��
? ? ?��______��
��3��д����Ӧ�۵����ӷ���ʽ______��
��4��д����C�μӵ���Cֻ����ԭ����������ԭ��Ӧ��ѧ����ʽ______��
��5����D��G��1��2����ڴ����������³�ַ�Ӧ��������ʣ�࣬��������Һ�����ʵ���������______?���÷�����ʾ����
�ο��𰸣�A�ڼ��ȵ�����������NaOH��Ӧ����DΪ��������̬���ʣ�˵��AΪ��Σ�DΪNH3��A�ֽ�õ������ʵ�����B��C��D��
BΪ������Ϊ���壬������þ��Ӧ������BΪCO2��C����������Ʒ�Ӧ������CΪH2O��GΪO2����AΪNH4HCO3��
������������Ӧ����NO��NO��������Ӧ����NO2��HΪNO��IΪNO2����JΪHNO3��þ�������̼��Ӧ����MgO��C��C��Ũ���ᷴӦ����CO2��NO2��H2O��EΪMgO��FΪ̼������ת����ϵ��
��1��������������֪��BΪCO2��̼ԭ������ԭ��֮���γ�2�Թ��õ��Ӷԣ��ṹʽΪO=C=O��DΪNH3��Nԭ���γ�3��N-H����������1�Թ¶Ե��ӣ���ȡsp3�ӻ������ӵĿռ乹��Ϊ�����ͣ��ʴ�Ϊ��O=C=O�������ͣ�
��2����Ӧ����þ�ڶ�����̼��ȼ����������þ��̼����Ӧ����ʽΪ��2Mg+CO2?��ȼ?.?2MgO+C��
��Ӧ����̼��Ũ���ᷴӦ���ɶ�����̼������������ˮ����Ӧ����ʽΪ��C+4HNO3 ��Ũ��?��?.?CO2��+4NO2��+2H2O��
�ʴ�Ϊ��2Mg+CO2?��ȼ?.?2MgO+C��C+4HNO3 ��Ũ��?��?.?CO2��+4NO2��+2H2O��
��3����Ӧ����̼��������������Ʒ�Ӧ���ɰ�����̼���ơ�ˮ�����ӷ���ʽΪ��NH4++HCO3-+2OH-�TNH3��+CO32-+2H2O��
�ʴ�Ϊ��NH4++HCO3-+2OH-�TNH3��+CO32-+2H2O��
��4����H2O�μ���ֻ����ԭ����������ԭ��Ӧ��Ϊ������ˮ��Ӧ����HF����������Ӧ����ʽΪ2F2+2H2O=4HF+O2��
�ʴ�Ϊ��2F2+2H2O=4HF+O2��
��5����NH3��O2��1��2����ڴ����������³�ַ�Ӧ��û��������ʣ�࣬�������ܷ�ӦʽΪ��NH3+2O2=HNO3+H2O�����ɵ�HNO3��H2O�����ʵ���֮��Ϊ1��1��������������Һ�����ʵ�����Ϊ6363+18��100%=79���ʴ�Ϊ��79��
���������
�����Ѷȣ�һ��
4������� ��12�֣��������е�A��B��C��D��E 5��Ԫ�أ�ԭ��������������A��Dͬ���壻A��B ��ԭ������֮�͵���C��ԭ��������C2?������D+���ӵĺ����������ȣ�Bԭ����D+���ӵĺ��������֮�͵���Eԭ�ӵĺ����������
��ԭ������֮�͵���C��ԭ��������C2?������D+���ӵĺ����������ȣ�Bԭ����D+���ӵĺ��������֮�͵���Eԭ�ӵĺ���������� ��D��E��Ԫ�����γ���������Ϊ1�U1�����ӻ����
��D��E��Ԫ�����γ���������Ϊ1�U1�����ӻ����
��1��EԪ�ص����ӽṹʾ��ͼΪ________��
��2��A��BԪ�ء�A��CԪ�ؾ��ɹ���18���ӵķ��ӣ��仯ѧʽ�ֱ�Ϊ______��_______��
��3��A��CԪ�ؿ����ԭ�Ӹ�����Ϊ1�U1�Ĺ��ۻ������ң���E����ͨ���ҵ�ˮ��Һ�У�����һ��ǿ�ᣬ��������ų�����Ӧ�Ļ�ѧ����ʽΪ?��
��4��A��B��C��D��E�е���������Ԫ�ؿ���ɶ��ֻ����X��Y�����е����֡�X��Y���ǼȺ����Ӽ��ֺ����ۼ������ӻ������X��Y�ֱ�����ˮʱ��X�ܴٽ�ˮ�ĵ��룬��Y������ˮ�ĵ��룬Xˮ��Һ��pH��7��Yˮ��Һ��pH��7��
��0.2mol��L?1��X��Һ��0.1mol��L?1��Y��Һ�������Ϻ���Һ�ʼ��ԡ����жϣ�
��X�Ļ�ѧʽΪ?��Y�Ļ�ѧʽΪ?��
�ڻ����Һ�и��ִ����������ʵ���Ũ���ɴ�С��˳��Ϊ?
?��
�ο��𰸣���12�֣���1��?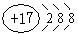 ?(2��)
?(2��)
��2��N2H4? (1��)? H2O2? (1��)
��3��Cl2+H2O2=2HCl+O2������HClO+H2O2=HCl+O2��+H2O�ɵ÷֣� (2��)
��4����NH4Cl(��NH4NO3) (2��)��NaOH (2��)��
��c(Cl?)��c(NH4+)��c(Na+)��c(OH?)��c(H+)
[��c(NO3?)��c(NH4+)��c(Na+)��c(OH?)��c(H +)](2��)
+)](2��)
�����������
�����Ѷȣ���
5������� ��5�֣���������ѧ��ѧ�г������ʵ�ת����ϵͼ�У���֪������AΪ����ɫ���塢BΪ�������ʣ�D��E��M�dz������嵥�ʣ�����MΪ����ɫ��N��θ����Ҫ�ɷ֣���ҵ����E��M����ȡN�����ƶϣ�
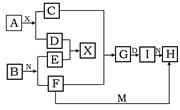
��1��д�����л�ѧʽ? A??I?
��2��Gת��ΪI������Ϊ?
��3��F+M��H���ӷ���ʽΪ?
��4��A+X��C+D�Ļ�ѧ����ʽΪ________________________
�ο��𰸣���1��Na2O2��Fe(OH)3����2����ɫ����Ѹ��ת��Ϊ����ɫ�����ת��Ϊ���ɫ��
��3��2Fe2����Cl2=2Fe3��?(4)2Na2O2��2H2O=4NaOH��O2��
���������MΪ����ɫ����M��������N��θ����Ҫ�ɷ֣���N���Ȼ��⡣AΪ����ɫ���壬���A�ǹ������ơ�BΪ�������ʣ���E��������F���������Լ�����Ӧ��˵��B�DZ�۽�������Ϊ��������F���Ȼ�������H���Ȼ�����D��������Ӧ������D��������X��ˮ��C���������ƣ�G��������������I������������
�����Ѷȣ�һ��