1��ѡ���� ���ڷ��õ�Ũ���᳣�Ի�ɫ���������еĻ�ɫ��õķ�����
A.�ڹ��մ�����
B.ͨ�������Ŀ���
C.��������ˮ
D.����Ư��
�ο��𰸣�B
���������
�����Ѷȣ�һ��
2��ѡ���� ����װ���ܴﵽʵ��Ŀ����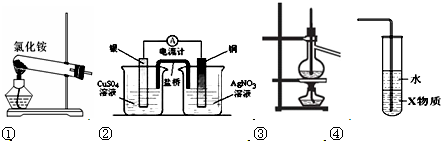
A.ʵ������װ�â���ȡ����
B.װ�âڽ���ѧ��ת��Ϊ����
C.װ�âۿ����ڷ���е����ϴ�Ļ���Һ������
D.װ�â���X��Ϊ���Ȼ�̼�����������հ���������ֹ����
�ο��𰸣�D
���������������A���Ȼ�������ֽ⣬�ڹܿڰ�����HCl���������Ȼ�泥�
B���뷴Ӧ�з�����ѧ��Ӧ�������γ�ԭ��أ�
C���¶ȼ�Ӧ��������ƿ��֧�ܿڴ���
D�����Ȼ�̼�ܶȴ����²㣬��ʹ������ˮ���룮
���A���Ȼ�������ֽ⣬�ڹܿڰ�����HCl���������Ȼ�泥����������Ȼ���Ʊ���������A����
B���뷴Ӧ�з�����ѧ��Ӧ�������γ�ԭ��أ�����ʵ�ֻ�ѧ��ת��Ϊ���ܣ���B����
C���¶ȼ�Ӧ��������ƿ��֧�ܿڴ����ⶨ��ֵ��¶ȣ���C����
D�����Ȼ�̼�ܶȴ����²㣬��ʹ������ˮ���룬�ɷ�ֹ��������D��ȷ��
��ѡD��
���������⿼�黯ѧʵ�鷽�������ۣ��漰������Ʊ���ԭ��ء�������װ�õȣ�����ʵ��Ļ��������ͷ�Ӧԭ���Ŀ��飬��Ŀ�ѶȲ���
�����Ѷȣ���
3��ѡ���� ijͬѧ�������ʵ�飬����m��ͭ���Ͻ���Ʒ��ͭ������������
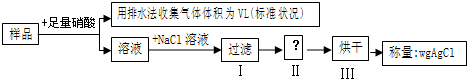
����˵���д������
A.�ռ�����V?L����Ϊ?NO
B.��ȱ�ٲ����ᵼ��ʵ����ƫС
C.��ͭ���Ͻ�ԭ���������Ϊ?
D.����m��V����ȷ��ͭ����������
�ο��𰸣�D
���������������A��������ͼ��֪��ʵ������ˮ���ռ����壬������������ˮ��Ӧ����NO���ʽ��������ᷴӦ�������岻����NO��NO2��NO��NO2������ռ�������ΪNO��
B��������ͼ��֪����Һ�м����Ȼ��ƣ���������ת��Ϊ�Ȼ���������ͨ���ⶨ�Ȼ�������������������������������������ͭ�ĺ��������������ڹ���֮���֮ǰ�����ڹ��˺���Ȼ�������һЩ���ӣ�Ӧϴ�Ӹ��ŵ����ʣ���ֹ�ⶨ���Ȼ�������������
C������ԭ������ȫ������ΪNO������NO�����ʵ������ٸ���Nԭ��ת���غ���㱻��ԭ�����
D��������ͼ��֪��ʵ��ԭ��Ϊ���ڷ�Ӧ����Һ�м����Ȼ��ƣ���������ת��Ϊ�Ȼ���������ͨ���ⶨ�Ȼ�������������������������������������ͭ�ĺ�����
���A��������ͼ��֪��ʵ����ˮ���ռ���������������ˮ��Ӧ����NO���ʽ��������ᷴӦ�������岻����NO��NO2��NO��NO2������ռ�������ΪNO����A��ȷ��
B��������ͼ��֪����Һ�м����Ȼ��ƣ��������� ת��Ϊ�Ȼ���������ͨ���ⶨ�Ȼ�������������������������������������ͭ�ĺ��������������ڹ���֮���֮ǰ�����ڹ��˺���Ȼ�������һЩ���ӣ�Ӧϴ�Ӹ��ŵ����ʣ���ֹ�ⶨ���Ȼ��������������ºϽ���������������ͭ������ƫС������ͭ�ĺ���ƫ�ͣ���B��ȷ��
C�����ɵ�������NO�����ʵ���Ϊ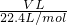 =
=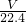 mol������ԭ��ת���غ��֪����ԭ������Ϊ
mol������ԭ��ת���غ��֪����ԭ������Ϊ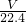 mol����C��ȷ��
mol����C��ȷ��
D���Ȼ���������Ϊwg������Ag�غ����Ͻ��������������Ͻ�������ȥAg������ΪCu������������ȷ��Cu��������������D����
��ѡD��
���������⿼��ѧ����ʵ��ԭ�������⡢������ɵIJⶨ�ȣ��Ѷ��еȣ�����ԭ���ǹؼ�����Ҫѧ��������ʵ�Ļ���֪ʶ���ۺ�����֪ʶ������������������
�����Ѷȣ�����
4��ѡ���� ijϡ��������11.2 gCuǡ����ȫ��Ӧ�������Ĵ�ϡ�����ں�Fe��Ӧͬ������NOʱ���������FeΪ
A.11.2 g
B.10.4 g
C.9.8 g
D.8.4 g
�ο��𰸣�C
���������
�����Ѷȣ�һ��
5��ѡ���� ����˵������ȷ����
A.A
B.B
C.C
D.D
�ο��𰸣�A
���������������A�����ϡ������Һ��ʵ���ϵ���ˮ����ҺŨ������
B���ɵ����ƶ������֪�����ӵ�Դ����������Ϊ���ص�������
C����Ϊԭ���װ�ã�FeΪ������PtΪ������
D������ԭ����������缫����ʽ��д�ܷ�Ӧʽ��
���A�����ϡ������Һ��ʵ���ϵ���ˮ������Ũ��������ҺpH��С����A����
B���ɵ����ƶ������֪�����ӵ�Դ����������Ϊ���ص�������������ӦΪ2Cl--2e-�TCl2������B��ȷ��
C����Ϊԭ���װ�ã�����������������ʴ��FeΪ������PtΪ����������������ԭ��Ӧ����ⷽ��ʽΪO2+2H2O+4e-�T4OH-����C��ȷ��
D��Fe3+�������õ��ӱ���ԭ��Cu�ڸ���ʧ���ӱ��������ܷ�ӦʽΪ2Fe3++Cu�TCu2++2Fe2+����D��ȷ��
��ѡA��
���������⿼�黯ѧʵ�鷽�������ۣ������ڵ绯ѧ֪ʶ�Ŀ��飬ע����յ��غ�ԭ��صĹ���ԭ�������յ缫����ʽ����д������
�����Ѷȣ���