1、选择题 下列有关氢化物的叙述中正确的是( )
A.稳定性:H2S>HF
B.HCl的电子式为
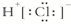
C.一个D2O分子所含的中子数为8
D.在卤化氢中HF最稳定
2、选择题 根据陈述的知识,类推得出的结论正确的是

A.HCl的水溶液显酸性,则NH3的水溶液也显酸性

B.常温下铝投入浓硫酸、浓硝酸中都没有气泡产生,则常温下铝投入浓盐酸中也没有气泡产生

C.常温下钠易与水反应,则常温下钾也易与水反应

D.无色的苯将橙色的溴水萃取后呈橙红色,则无色的苯将黄色的碘水萃取后呈棕黄色
3、填空题 (4分)一些老式建筑的下水道都是铁管铺设的,若将实验室的废盐酸倒入下水道将会发生反应(写化学方程式,下同)?,
导致铁管腐蚀;农药波尔多液中含有CuSO4,所以这种农药不能用铁制品盛装,否则会发反应? ??而使铁制品腐蚀;?
??而使铁制品腐蚀;?
热水 瓶胆上水垢的主要成分是Mg(OH)2和CaCO3两种物质,在实验室除去它们最好选择的反应是?
瓶胆上水垢的主要成分是Mg(OH)2和CaCO3两种物质,在实验室除去它们最好选择的反应是?
4、推断题 A、B、C、D、E为五种短周期元素,其中A、B、C位于同一周期,A元素的气态氢化物足一种广泛应用的优质气体燃料,B元素的氢化物是用途最为广泛的溶剂。B元素可分别与A、C、D、E组成HB2型化合物,已知在DB2中,D与B的质量比为7:8;在EB2中,E与B的质量比为1:1。根据以上条件回答下列问题:
(1)请写出C单质分子的电子式_______;DB2晶体中化学键的类型为______;写出AE2的结构式_______。
(2)C的气态氢化物易液化,原因是:____________________。
(3)C和D结合可生成一种超硬物质,有关该物质性质的叙述中不正确的是___________。
①有润滑性 ②易磨损 ③抗腐蚀 ④强还原性 ⑤抗冷热
(4)B元素可分别与A、E形成多种阴离子。某溶液是由其中若干种阴离子组成的无机盐溶液,为了检验该溶液中的阴离子,分别取两份溶液进行如下实验:
①第一份溶液中加入足量盐酸,只产生无色气体;
②第二份溶液中加入足量的BaCl2溶液,有白色沉淀产生,再加入足量的稀硝酸,白色沉淀质量减少。
由此得出的结论是___________________
(5)E元素的一种氧化物可与过氧化钠及氯水发生氧化还原反应。 该氧化物与过氧化钠反应的化学方程式为_____________________;该氧化物与氯水反应的离子方程式为_____________________。
5、选择题 下列说法正确的是
A.原子最外层电子数为2的元素一定是金属元素
B.元素周期表中所有元素都是从自然界中发现的
C.过渡元素不全是金属元素
D.常温常压下,、气态单质的分子都是由非金属元素的原子形成的