1������� �����仯�������ճ����������Ӧ�ù㷺���о������仯�����Ӧ�������ش�
I��ˮ��ľ�������ˮ�Ĵ����������仯����������أ�
��1������ˮ�����ø������ƣ�Na2FeO4������ˮ�ʣ�����������������ɱ������ͬʱ����ˮ���õ�ԭ���� ����
��2����ʽ������[Fe��OH��SO4]��һ��������ˮ����������Ч����������ҽҩ��Ҳ���������������������Ѫ����ҵ�����÷���м�����������������������ȣ�������ʽ�������Ĺ����������£�
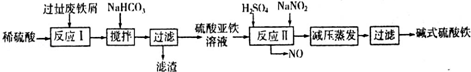
��֪������������������������ʽ����ʱ��Һ��pH���±���
������
| Fe��OH��3
| Fe��OH��2
| Al��OH��3
|
��ʼ����
| 2.3
| 7.5
| 3.4
|
��ȫ����
| 3.2
| 9.7
| 4.4
|
�ش��������⣺
��д����ӦI����Ҫ������������ԭ��Ӧ�����ӷ���ʽ�� ����
�ڼ�������NaHCO3��Ŀ���ǵ�����ҺpH��Ӧ����pH�ķ�ΧΪ�� ����
����ʵ�������У���ӦII��ͬʱͨ��O2�Լ���NaNO2����������ͨ��5.6L O2����״���������൱�ڽ�ԼNaNO2������Ϊ�� ��g��
�ܼ�ʽ����������ˮ�������[Fe��OH��]2+���ӣ��ɲ���ˮ������[Fe2��OH��4]2+�ۺ����ӣ���ˮ�ⷴӦ�����ӷ���ʽΪ�� ����
II���Ļ�����Ҳ���Ʊ�����﮵�ص���Ҫԭ�ϣ���֪��������﮵���ܷ�ӦΪ��FePO4+Li LiFePO4������еĹ������ʿɴ���Li+����д���õ�س��ʱ��������Ӧʽ�� ����
LiFePO4������еĹ������ʿɴ���Li+����д���õ�س��ʱ��������Ӧʽ�� ����
�ο��𰸣���1��FeO42
���������
�����Ѷȣ�����
2������� (13��)��.һ����̼��һ����;�൱�㷺�Ļ�������ԭ�ϡ�
(1)�������з�Ӧ���Խ�����ת��Ϊ���ȴ�99.9%�ĸߴ�����
Ni(s)��4CO(g) Ni(CO)4(g) �÷�Ӧ�Ħ�H? ��?0 (ѡ�������������)��
Ni(CO)4(g) �÷�Ӧ�Ħ�H? ��?0 (ѡ�������������)��
(2)�ڸ�����һ����̼�ɽ���������ԭΪ��������֪��
C(s)��O2(g)��CO2(g)? ��H1����393.5 kJ��mol��1
CO2(g)��C(s)��2CO(g)?��H2��+ 172.5 kJ��mol��1
S(s)��O2(g)��SO2(g)?��H3����296.0 kJ��mol��1
��д��CO��SO2���Ȼ�ѧ����ʽ?��?��
(3)��ͼ����ͼ��һ̼����ȼ�ϵ�أ�����COΪȼ�ϣ�һ������Li2CO3��Na2CO3���ۻ����Ϊ����ʣ���ͼ�Ǵ�ͭ������װ��ͼ������ȼ�ϵ��Ϊ��Դ���д�ͭ�ľ���ʵ�顣�ش��������⣺
��д��A�������ĵ缫��Ӧʽ?��?��
��Ҫ��ȼ�ϵ��Ϊ��Դ���д�ͭ�ľ���ʵ�飬��B��Ӧ������?��(���C����D��)������
�۵�����2.24 L(�����)COʱ����ͭ�缫�����ϼ���ͭ������? ��?(������ڡ��������ڡ� ��С�ڡ�)6.4�ˡ�

��.(1)��֪Na2CrO4��Һ�ữʱ�����ķ�ӦΪ��2CrO42����2H�� Cr2O72����H2O����1L�ữ��������Һ�и�Ԫ�ص������ʵ���Ϊ0.55 mol��CrO42����10/11ת��ΪCr2O72������֪������ʱ�÷�Ӧ��ƽ�ⳣ��K��1014�������ữ��������Һ��pH��?��?��
Cr2O72����H2O����1L�ữ��������Һ�и�Ԫ�ص������ʵ���Ϊ0.55 mol��CrO42����10/11ת��ΪCr2O72������֪������ʱ�÷�Ӧ��ƽ�ⳣ��K��1014�������ữ��������Һ��pH��?��?��
(2)�����йع��ұ�����CrO42���ķ�ˮҪ����ѧ������ʹ��Ũ�Ƚ���5.0��10��7 mol��L��1���²����ŷš���CrO42���ķ�ˮ����ͨ�����������ַ�����
�ٳ���������������Ա�������BaCrO4������Ksp(BaCrO4)��1.2��10��10�ݣ��ټ�������������δ��������Ba2������������Ա��κ�ķ�ˮ��Ba2����Ũ��Ӧ��С��?��?mol��L��1��Ȼ���ٽ��к����������ܴﵽ�����ŷű���
�ڻ�ԭ����CrO42�� Cr3��
Cr3�� Cr(OH)3���ø÷�������10 m3 CrO42�������ʵ���Ũ��Ϊ1.0��10��3 mol��L��1�ķ�ˮ��������Ҫ�̷�(FeSO4��7H2O����Է�������Ϊ278)?�� ?Kg(������λС��)��
Cr(OH)3���ø÷�������10 m3 CrO42�������ʵ���Ũ��Ϊ1.0��10��3 mol��L��1�ķ�ˮ��������Ҫ�̷�(FeSO4��7H2O����Է�������Ϊ278)?�� ?Kg(������λС��)��
�ο��𰸣���13�֣���.��1������1�֣�
��2��2CO(g)��SO2(g)��S(s)��2CO2(g)?��H����270 kJ��mol��1��2�֣�
��3����CO ��2e�� + CO3 2�D��2CO2?��2�֣��� D��1�֣�?��С�ڣ�1�֣�
��.��1�� 6?��2�֣�
��3��2.4��10��4��2�֣�? 8.34��2�֣�
�����������
�����Ѷȣ�һ��
3��ѡ���� ��ʯī���缫���������Һ��������֮����ʣ�����Һ�м�����������ˮ����ʹ��Һ�͵��ǰ��ȫ��ͬ����
[? ]
A. NaCl
B. H2SO4
C. CuCl2
D. AgNO3
�ο��𰸣�B
���������
�����Ѷȣ�һ��
4������� ������ͼ�ش��������⣺

��A��B��Ϊ̼������������Һ��������
��1����װ���� �أ���װ���� ����Fe��Ϊ ����A��Ϊ ��
��2��A���ĵ缫��Ӧ
��3�����׳���Fe�ܽ�0��3 mol�����ҳ��в���������������״����Ϊ L��
�ο��𰸣���1��ԭ��أ����أ����������� ��2��2Cl��---2e- == Cl2�� ��3��6��72
�����������1��ԭ�����һ�����2�����Բ�ͬ�����������Ը�װ���м׳���ԭ��أ����ǵ��أ�����������ͭ����������A��������
��2��A����������������Ӧ�������ӷŵ磬���������ӵõ��������������缫��ӦʽΪ2Cl��---2e- == Cl2����
��3�����׳���Fe�ܽ�0��3 mol����װ����ת��0��6mol���ӣ��ҳ���ֻ��A������0��3mol��������״���µ������0��3mol��22��4L/mol=6��72L��
���㣺����Ե绯ѧװ�õ��жϣ��绯ѧԭ����Ӧ��
�����Ѷȣ�����
5��ѡ���� ��--��(Ni--Cd)�ɳ���ؿ��Է������·�Ӧ��
Cd(OH)2 + 2Ni(OH)2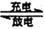 Cd + 2NiO(OH)+ 2H2O
Cd + 2NiO(OH)+ 2H2O
�ɴ˿�֪���õ�س��ʱ�������ǣ�?����
A��Cd
B��NiO(OH)
C��Cd(OH)2
D��Ni(OH)2
�ο��𰸣�D
�����������������������Ӧ�����ϼ����ߣ���ѡD��
���������⿼����ǵ��ԭ����Ӧ�ã��ѶȲ���ּ�ڿ���ѧ���Ի���֪ʶ�����������
�����Ѷȣ���