1��ѡ���� ��һ�������£�RO3n-��I-�ɷ������·�Ӧ��RO3n-+6I-+6H+ = R-+ 3I2 +3H2O����RO3n-��RԪ�صĻ��ϼ�Ϊ
[? ]
A����1
B����3
C����5
D����7
�ο��𰸣�C
������������������ӷ���ʽǰ����ѭ����غ㣬����n=1�����ݻ��ϼ۹���RO3-����Ԫ�ػ��ϼ�Ϊ-2�ۣ�����RԪ�صĻ��ϼ�Ϊ+5�ۣ�
���Դ�ѡC
�����Ѷȣ���
2��ѡ���� ��֪M2O7x-+3S2-+14H+=2M3++3S��+7H2O����M2O7x-�е�M�Ļ��ϼ�Ϊ��������
A��+2
B��+3
C��+4
D��+6
�ο��𰸣�M2O7x-+3S2-+14H+=2M3++3S��+7H2O�У�
�ɵ���غ��֪��
��-x��+3����-2��+14����+1��=2����+3����
���x=2��
��M2O72-�е�M�Ļ��ϼ�Ϊy��
��y��2+��-2����7=-2��
���y=+6��
��ѡD��
���������
�����Ѷȣ�һ��
3��ѡ���� ���б仯��Ҫ��������������ʵ�ֵ��ǣ�������
A��CaCO3��CO2
B��KMnO4��O2
C��HCl��Cl2
D��H2SO4��H2
�ο��𰸣�A��CaCO3��CO2��Ԫ�صĻ��ϼ�û�б仯�����跢��������ԭ��Ӧ����A��ѡ��
B��KMnO4��O2��OԪ�صĻ��ϼ����ߣ�����������ԭ��Ӧ��������Ҫ�������������ȷֽ⼴��ʵ�֣���B��ѡ��
C��HCl��Cl2��ClԪ�صĻ��ϼ����ߣ�����Ҫ�����������ܷ�������Cѡ��
D��H2SO4��H2��HԪ�صĻ��ϼ۽��ͣ�����Ҫ�ӻ�ԭ�����ܷ�������D��ѡ��
��ѡC��
���������
�����Ѷȣ�һ��
4������� ��֪ij��Ӧ�з�Ӧ�����������У�HNO3��Cu��NO3��2��NO��Cu��H2O
��1����֪Cu�ڷ�Ӧ��ʧȥ���ӣ���÷�Ӧ����������______��
��2���÷�Ӧ�У�������ԭ��Ӧ�Ĺ����ǣ�д��ѧʽ��______��______��
��3������Ӧ��Ļ�ѧʽ������ƽ���ϵ���������з����У����������ת�Ƶķ������Ŀ��
��4������1.5mol?Cu�μӷ�Ӧ����______mol?HNO3�μӷ�Ӧ������ԭ��HNO3�����ʵ�����______mol��ת�Ƶ��ӵ����ʵ�����______?mol��
�ο��𰸣���1��Cu�ڷ�Ӧ��ʧȥ���ӣ����Խ���ͭ�ǻ�ԭ����HNO3�е�NԪ�ش�����ۣ�����������������ԣ������������ʴ�Ϊ��HNO3��
��2���÷�Ӧ�ǽ���ͭ������ķ�Ӧ�����ϼ۽��͵�NԪ�ط�����ԭ��Ӧ�����������+5�۵�Ԫ�ؽ�ΪNO�е�+2�۵�Ԫ�أ��ʴ�Ϊ��HNO3��NO��
��3���÷�Ӧ�ǽ���ͭ������ķ�Ӧ�����ݵ����غ�����ƽ��ѧ����ʽΪ��3Cu+8HNO3�T3Cu��NO3��2+2NO��+4H2O������ת�Ƶķ������Ŀ������ʾ��
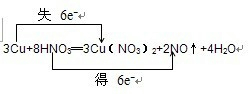
����

���ʴ�Ϊ��

��
��4�����ݻ�ѧ����ʽ���Կ���������3mol����ͭ�μӷ�Ӧʱ������8mol��������뷴Ӧ��ת�Ƶ���Ϊ6mol�����Ե���1.5mol����ͭ�μӷ�Ӧʱ������4mol��������뷴Ӧ������ԭ��HNO3�����ʵ����Dzμӷ�Ӧ�������ʵ������ķ�֮һ��������ԭ��HNO3�����ʵ�����1mol��ת�Ƶ���Ϊ3mol���ʴ�Ϊ��4��1��3��
���������
�����Ѷȣ�һ��
5��ѡ���� ij�����������ڹ����¿����ɾ��к�ǿ�������������ʣ�����������������ˮ���е���Ⱦ������йظý����������Ӧ����������ȷ���ǣ�������
A����������SO2������SO3
B����װ�Ҿ��ͷų����ļ�ȩ������CO2��ˮ
C����ҽҩ��ˮ�еı���������CO2��ˮ
D������Ʒ�ˮ�е������CNһ��������CO2��N2
�ο��𰸣������Ϣ�����������ֽ�����������ת���ɾ��к�ǿ�������������ʣ�������������������ˮ���е���Ⱦ����������ʣ�
A�������ʰ�SO2����ΪSO3�Բ�������������Ⱦ����������������������A����
B���ؼ�������к�ǿ�������ԣ���������ȩΪ������̼��ˮ����B��ȷ��
C��C6H5OH�л�ԭ�ԣ����������������CO2��ˮ����C��ȷ��
D��CN-���Ӿ��л�ԭ�ԣ�������ΪCO2��N2����D��ȷ��
��ѡA��
���������
�����Ѷȣ���