1、填空题 将0.1mol某烃的衍生物与标准状况下4.48L氧气混合于一密闭容器中,点火后发生不完全燃烧,得到CO、CO2和H2O的气态混合物,将混合物通过浓硫酸时,浓硫酸的质量增加了3.6g,通过足量澄清石灰水,可得经干燥后的沉淀10g,剩余气体与灼热的氧化铁充分反应后再通入澄清石灰水时,可得经干燥后的沉淀20g.?
求:
(1)该有机物的化学式;
(2)该有机物可与醇发生酯化反应,且可使溴水褪色,写出该有机物的结构简式.
参考答案:(1)0.1mol烃和4.48L及0.2mol氧气反应,生成水的质量是3.6g,即生成水的物质的量是0.2mol,所以有机物中H的物质的量为0.4mol,通过足量澄清石灰水,可得干燥后的沉淀10g,根据CO2~CaCO3,所以二氧化碳的物质的量是0.1mol,一氧化碳与灼热的氧化铁充分反应后再通入澄清石灰水时,可得经干燥后的沉淀20g,根据CO~CO2~CaCO3,所以生成一氧化碳的物质的量是0.2mol,则有机物中含C的物质的量是0.3mol,根据氧原子守恒,含有氧原子的物质的量为:0.2mol+0.1mol×2+0.2mol-0.2mol×2=0.2mol,有机物中C、H、O的原子个数比是3:4:2,分子式为:C3H4O2,
答:该有机物的化学式为C3H4O2;
(2)有机物可与醇发生酯化反应,则含有羧基,且可使溴水褪色,含有碳碳双键,所以有机物的结构简式为:
CH2=CHCOOH,
答:该有机物的结构简式为CH2=CHCOOH.
本题解析:
本题难度:简单
2、选择题 某物质的分子式为CxHyOz,取该物质ag在足量的O2中充分燃烧后,将产物全部通入过量的Na2O2中,若Na2O2固体的质量增加了bg,并且a<b,则x、y、z必须满足的关系是
[? ]
A.x>z
B.x=y=z
C.x=z
D.x<z
参考答案:A
本题解析:
本题难度:一般
3、选择题 现有乙酸、乙烯和丙烯(C3H6)的混合物,其中氧的质量分数为a,则碳的质量分数是
[? ]
A.
B.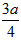
C.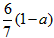
D.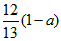
参考答案:C
本题解析:
本题难度:一般
4、填空题 已知某烃A含碳元素的质量分数为85.7%。结合以下信息回答问题:
(1)若烃A密度是相同状况下氢气密度的42倍。则烃A的相对分子质量_____________,分子式为_____________。
(2)若烃A可作果实催熟剂。则由A制取高分子化合物的化学方程式为________________________A和水在一定条件下反应生成B。B为生活中常见的有机物,B可与另一种生活中常见有机物在一定条件下反应生成有香味的物质C,写出生成C的化学方程式_____________________________
参考答案:(1)84;C6H12
(2)nCH2=CH2
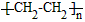 ;CH3COOH+C2H5OH
;CH3COOH+C2H5OH CH3COOC2H5+H2O
CH3COOC2H5+H2O
本题解析:
本题难度:一般
5、计算题 有机物A由碳、氢两种元素组成.现取0.2 mol A与一定量氧气(标准状况)在密闭容器中燃烧,燃烧后生成二氧化碳、一氧化碳和水蒸气(假设反应物没有剩余).将反应生成的气体依次通过浓硫酸、碱石灰和灼热的氧化铜,浓硫酸增重18g,碱石灰增重26.4g,氧化铜固体质量减少3.2g.回答下列问题:
(1)通过计算确定该有机物的分子式。
(2)写出符合上述条件的有机物的结构简式。
参考答案:(1) 浓硫酸吸水,水的质量为18g,水的物质的量为1mol,
氢原子的物质的量为2mol 碱石灰吸收二氧化碳,二氧化碳的质量为26.4g,
二氧化碳的物质的量为0.6mol,碳原子的物质的量为0.6mol
一氧化碳与氧化铜按照物质的量1:1反应,每有1mol氧化铜反应,氧化铜质量减少16g,
可求一氧化碳的物质的量为0.2mol,碳原子的物质的量为0.2mol
根据碳氢元素守恒,可求有机物分子式为C4H10
(2) 
本题解析:
本题难度:困难