1、选择题 四种短周期主族元素A、B、C、D的原子序数依次增大,它们的原子序数之和为36,最外层电子数之和为14;A、C原子的最外层电子数之和等于B原子的次外层电子数。下列叙述不正确的是
A.A、B、D三种元素形成的化合物中一定有强酸
B.B元素在地壳中的含量一定最高
C.C元素在元素周期表中一定位于第三周期第ⅠA族
D.D元素与氢元素形成化合物的化合物常温下一定为气体
参考答案:B
本题解析:短周期元素A、B、C、D的原子序数依次增大,它们的原子序数之和为36,最外层电子数之和为14;A、C原子的最外层电子数之和等于B原子的次外层电子数。如果B是第三周期元素,则C、D也一定是第三周期元素,因此BCD三种元素的原子序数之和一定是≥36,不符合同意。所以B是第二周期元素,则A、C原子的最外层电子数之和等于2,即都是第IA族元素,所以A是氢元素,C是钠元素。B、D的原子最外层电子数之和是14-2=12。二者的原子序数之和=36-1-11=24,因此符合条件的有氧元素和硫元素或者氮元素和氯元素,即B是氧元素或氮元素,D是硫元素或氯元素。
A为氢元素、B为氧元素、D为硫元素,三元素形成的酸有硫酸、亚硫酸,硫酸是强酸,亚硫酸是中强酸,故选项A正确;若B为氮元素,在地壳中的含量不处于第一位,故选项B不正确;钠元素位于第三周期第ⅠA族,选项C正确;H2S或氯化氢均是气体,选项D正确,答案选B。
点评:该题是高考中的常见题型,属于中等难度的试题。试题基础性强,侧重对学生基础知识的巩固和训练,有利于提高学生的逻辑推理能力和应试能力。本题主要是元素“位、构、性”三者关系的综合考查,比较全面考查学生有关元素推断知识和灵活运用知识的能力,考查了学生对物质结构与性质关系以及运用元素周期律解决具体化学问题的能力。利用提供数据及位置关系推断元素是解题的关键,难点是B和D元素的推断。
本题难度:简单
2、填空题 A、B、C三种元素为短周期元素,A元素的阴离子不能被任何氧化剂氧化,则A离子的结构示意图为___________,它是___________离子。1 mol B单质能从盐酸中置换出3 g氢气,此时B转变为与Ne原子具有相同电子层结构的离子,则B元素是___________;B的最高价氧化物对应水化物的化学式为___________。C元素有3个电子层,且最外电子层比L层少2个电子,则C元素是___________;C与Na反应后生成物的电子式为___________,化合物中的化学键属于___________。
参考答案: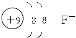 ?铝? Al(OH)3?硫
?铝? Al(OH)3?硫
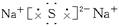 ?离子键
?离子键
本题解析:A元素的阴离子不能被任何氧化剂氧化,说明A元素是非金属性最强的元素,则A为氟元素,其阴离子即为F-,结构示意图为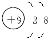 。
。
n(H2)=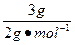 =1.5mol,因为
=1.5mol,因为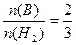 ,所以B为+3价的金属,又因B转变为与Ne原子的电子层结构相同的离子,则B元素为铝元素;由题意知C元素原子的最外层(M层)上有6个电子,故C为硫元素,它与钠反应后生成离子化合物硫化钠,含有离子键,其电子式为
,所以B为+3价的金属,又因B转变为与Ne原子的电子层结构相同的离子,则B元素为铝元素;由题意知C元素原子的最外层(M层)上有6个电子,故C为硫元素,它与钠反应后生成离子化合物硫化钠,含有离子键,其电子式为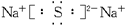 。
。
本题难度:简单
3、选择题 短周期元素甲,乙,丙,丁的原子序数依次增大,甲和乙形成的气态化合物的水溶液呈碱性,乙位于第VA族,甲和丙同主族,丁原子最外层电子数和电子层数相等,则? (? )
A.原子半径:丙>丁>乙
B.单质的还原性:丁>丙>甲
C.甲,乙,丙的氧化物均为共价化和物
D.乙,丙,丁的最高价氧化物对应的水化物能相互反应
参考答案:AD
本题解析:短周期元素甲乙丙丁的原子序数依次增大,甲和乙形成的气态氢化物的水溶液呈碱性,则甲为H,乙位于第VA族,乙为N;甲和丙同主族,丙为Na;丁的最外层电子数和电子层数相等,则丁在第三周期第ⅢA族,即丁为Al,A、同周期原子半径从左向右减小,电子层越多,半径越大,则原子半径为丙>丁>乙,故A正确;B、金属性越强,单质的还原性越强,则单质的还原性丙>丁>甲,故B错误;C、甲、乙的氧化物为共价化合物,丙的氧化物为离子化合物,故C错误;D、乙、丙、丁的最高价氧化物对应的水化物分别为硝酸、氢氧化钠、氢氧化铝,氢氧化铝为两性氢氧化物,能相互反应,故D正确;故选D。
本题难度:一般
4、选择题 下列各组物质中,前者是混合物,后者是单质的是
A.Na2CO3・10H2O、Na2CO3
B.碳酸氢铵、液氨
C.石油、液氢
D.碘酒、干冰
参考答案:C
本题解析:A项,两者都是化合物;B项,都是化合物;C项,石油是混合物,液氢是单质;D项,前者是混合物,后者是化合物.
本题难度:困难
5、选择题 X、Y、Z、R分别代表4种元素。a、b、c、d分别是aXm+、bYn+、cZm-、dRn-离子的核电荷数,已知aXm+、bYn+、?cZm-、dRn-离子具有相同的电子层结构,则下列关系正确的是(?)
A.a-c="2n"
B.a-b="n-m"
C.c-d="m+n"
D.b-d=2n
参考答案:D
本题解析:原子aX(或bY)的核外电子数为a(或b),阳离子aXm+(或bYn+)是其原子aX(或bY)失去m个(或n个)电子生成的,其核外电子数为a-m(或b-n)。原子cZ(或dR)的核外电子数为c(或d),阴离子cZm-(或dRn-)是其原子cZ(或dR)得到m个(或n个)电子生成的,其核外电子数为c+m(或d+n)。以上结论也可根据阴加阳减规律快速得出。
由于aXm+、bYn+、cZm-、dRn-离子具有相同的电子层结构,即它们的电子层数和对应电子层上的电子数都相等,故核外电子总数也相等。则a-m=b-n=c+m=d+n。
由“a-m=c+m”可以看出A不正确,由“a-m=b-n”可以看出B不正确,由“c+m=d+n”可以看出C不正确,由“b-n=d+n”可以看出D正确。
本题难度:简单