1、选择题 X、Y、Z、W为四种短周期主族元素,其中X、Z同族,Y、Z同周期,W是短周期主族元素中原子半径最大的,X原子最外层电子数是核外电子层数的3倍,Y的最高正价与最低负价代数和为6.下列说法正确的是( )
A.Y元素最高价氧化物对应的水化物化学式H2YO4
B.原子半径由小到大的顺序为:X<Z<Y
C.Y、Z两种元素气态氢化物中,Z的气态氢化物最稳定
D.X与W形成的两种化合物中,阴、阳离子物质的量之比均为1:2
参考答案:X、Y、Z、W为四种短周期主族元素,W是短周期主族元素中原子半径最大的,则W为Na元素;X原子最外层电子数是核外电子层数的3倍,只能为电子层数为2,最外层电子数为6,即X为O元素,X、Z同族,则Z为S元素;Y的最高正价与最低负价代数和为6,其最高价为+7价,Y、Z同周期,Y为Cl元素,
A.Y为Cl,Y元素最高价氧化物对应的水化物化学式HYO4,故A错误;
B.电子层越多,半径越大,同周期从左向右原子半径在减小,则原子半径由小到大的顺序为:X<Y<Z,故B错误;
C.非金属性Cl>S,则Y、Z两种元素气态氢化物中,Y的气态氢化物最稳定,故C错误;
D.X与W形成的两种化合物为Na2O、Na2O2,阴、阳离子物质的量之比均为1:2,故D正确;
故选D.
本题解析:
本题难度:简单
2、选择题 下列说法错误的是(?)
A.附着在试管内壁上的AgCl固体可用氨水溶解而洗去
B.可用氨水鉴别AlCl3、AgNO3和CuSO4三种溶液
C.向氨水中滴加CuSO4溶液至过量,先产生蓝色沉淀,然后沉淀溶解并得到深蓝色溶液
D.加热碘单质,产生紫色碘蒸气,这个过程只克服范德华作用力
参考答案:C
本题解析:氯化银能溶于氨水形成配合物,A正确。氨气能和银离子、铜离子形成配合物,但氨水不能溶解氢氧化铝,所以B正确。C不正确,应该是向硫酸铜溶液中滴加氨水至过量,先产生蓝色沉淀,然后沉淀溶解并得到深蓝色溶液。碘属于分子晶体,升华破坏的是分子间作用力,D正确。所以答案选C。
本题难度:一般
3、选择题 下列有关化学用语或化学模型正确且能确定为对应物质的是( )
A.

甲烷
B.

二氧化碳
C.
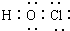
次氯酸
D.

NH4Cl
参考答案:AC
本题解析:
本题难度:一般
4、选择题 2001年11月17日,意大利一所大学的科学家使用普通氧分子和带正电荷的氧离子制造出了由4个氧原子构成的氧分子(O4),并用质谱仪探测到了它存在的证据。若该氧分子具有空间对称结构,则下列关于该氧分子的说法中正确的是
[? ]
A.该分子是氧元素的一种同位素
B.该物质与臭氧互为同素异形体
C.合成O4的反应属于核反应
D.该分子是由极性键构成的极性分子
参考答案:B
本题解析:
本题难度:简单
5、选择题 下列电子式中,书写正确的是( )
A.氮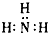
B.氯化氢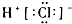
C.氮气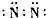
D.氯化镁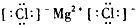
参考答案:A.氮原子为成键的孤对电子未画出,氨气分子中氮原子与氢原子之间形成1对共用电子对,电子式为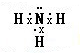 ,故A错误;
,故A错误;
B.HCl属于共价化合物,不存在离子键,分子中氢原子与氯原子之间形成1对共用电子对,HCl电子式为 ,故B错误;
,故B错误;
C.氮气分子中氮原子之间形成3对共用电子对,电子式为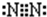 ,故C错误;
,故C错误;
D.氯化镁属于离子化合物,由镁离子与氯离子构成,电子式为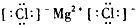 ,故D正确;
,故D正确;
故选D.
本题解析:
本题难度:简单