1、选择题 已知aA+、bB2+、cC-、dD2-四种离子均具有相同的电子层结构,关于A、B、C、D四种元素的叙述正确的是(?)
A. 原子半径:A>B>C>D? B. 原子序数:b>a>c>d
C. 离子半径:D>C>B>A? D. 失电子能力:B>A,得电子能力:D>C?
2、计算题 (4分)某金属重4 g,其原子核外有2 mol电子,核内共有1.204×1024个中子,该金属与足量盐酸反应,有0.2 mol电子发生转移,生成了6.02×1022个阳离子。
(1)该金属元素符号是________________,摩尔质量是____________。
(2)原子核内有____________个质子,____________个中子。
3、填空题 (共14分)下表是元素周期表中的一部分,根据A―I在周期表中的位置,用元素符号或化学式回答下列问题:
| ⅠA
| ?
| ?
| ?
| ?
| ?
| ?
| 0
|
1
| ?
| ⅡA
| ⅢA
| ⅣA
| ⅤA
| ⅥA
| ⅦA
| ?
|
2
| ?
| ?
| ?
| D
| E
| ?
| G
| I
|
3
| A
| B
| C
| ?
| F
| ?
| H
| ?
|
(1)表中元素,化学性质最不活泼的是?,氧化性最强的单质是?,还原性最强的单质是?;
(2)最高价氧化物的水化物碱性最强的是?,酸性最强的是?,呈两性的是?;
(3)要证明A、B、C的金属活泼性,可以用什么实验来证明,试举一例
实验操作?;
实验现象:?;
有关化学方程式:?
?
(4)G与H的气态氢化物稳定性?>?,说明相应单质的非金属性?>?。
4、选择题 下列叙述正确的是?
A.人们已经发现了109种原子

C.H,D,H+,H-,T都是氢元素的微粒
D.最外层电子数相同的微粒化学性质相似
5、填空题 X、Y、Z、W为按原子序数由小到大排列的四种短周期元素,已知:
①X元素原子价电子排布式为ns2np2,且原子半径是同族元素中最小的。
②Y元素是地壳中含量最多的元素;W元素的电负性略小于Y元素,在W原子的电
子排布中,p轨道上只有1个未成对电子。
③Z+与Y 2-具有相同的电子层结构;
请回答:
(1)Z2Y2的电子式为?,含有的化学键类型为?,Z2Y2为?晶体。
(2)X、Y、Z三种元素所形成的常见化合物的名称为?;XY2的结构式为?,分子的立体构型为?。
(3)X、Y、Z、W四种元素所形成的单质中,熔点最高、硬度最大的是?(填名称);晶体ZW的熔点比晶体XW4明显高的原因是?。
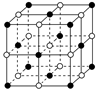
(4)ZW晶体的结构示意图如图。已知:ZW晶体的密度为ρ,摩尔质量为M,阿伏伽德罗常数为NA,则ZW晶体中两个最近的Z离子中心间的距离d可以表示为d=?。