1、选择题 有一澄清透明溶液,只可能含有大量H+、Fe3+、Fe2+、Al3+、AlO2-、CO32-、NO3-七种离子中的几种,向溶液中逐滴加入一定量1mol/L的NaOH溶液的过程中,开始没有沉淀,而后有沉淀,沉淀达最大量后继续滴加NaOH溶液沉淀部分消失.下列判断正确的是( )
A.一定不含Fe3+和Fe2+
B.一定含有Al3+,Fe3+、Fe2+至少含有一种或两种皆有
C.溶液可能含有NO3-
D.一定含有Fe3+,但一定不含Fe2+
参考答案:向该溶液中加入一定量1mol/L NaOH溶液的过程中,开始没有沉淀,说明溶液呈酸性,则一定含有大量的H+离子,
在酸性溶液中AlO2-、CO32-离子分别与H+离子反应生成Al(OH)3沉淀、CO2气体而不能存在,
根据溶液的电中性可知一定含有阴离子,则只有NO3-离子符合;
而后才有沉淀.能够生成沉淀的是Fe3+离子、Fe2+离子或Al3+离子中的一种或几种,但在酸性条件下Fe2+离子与NO3-离子发生氧化还原反应而不能共存,则一定不含Fe2+离子,沉淀达最大量后继续滴加NaOH溶液沉淀部分消失.说明一定含有Al3+和Fe3+;
综上所述,溶液中一定含有H+离子、NO3-离子,一定没有AlO2-、CO32-、Fe2+离子,一定含有Fe3+离子、Al3+;
A、依据判断可知一定含Fe3+离子,一定不含有Fe2+离子,故A错误;
B、根据分析判断结果可知Fe2+离子一定不存在,故B错误;
C、依据分析和溶液中电荷守恒可知,阴离子只有NO3-离子,所以一定存在NO3-离子,故C错误;
D、分析判断可知溶液中一定含有Fe3+,但一定不含Fe2+,故D正确;
故选D.
本题解析:
本题难度:简单
2、选择题 下列各组物质,用一种试剂无法区别的是
[? ]
A. FeCl2、AgNO3、Na2CO3、Na2SO3
B. NaNO3、AlCl3、NaCl、MgCl2
C. 苯、己烯、四氯化碳、乙醇
D. (NH4)2SO4、NH4Cl、Na2SO4、NaCl
参考答案:B
本题解析:
本题难度:一般
3、填空题 I.甲、乙、丙、丁、戊分别是Na2SO4、Ba(?NO3)2、HNO3、BaCl2、NaOH五种溶液中的一种,现利用X(一种钠 ?盐)溶液鉴别它们,已知气体B的密度在同温同压下是氢气密度的22倍。试根据下图中的转化关系回答下列问题:?
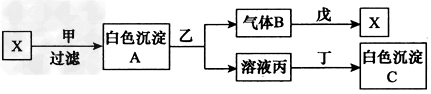
(1)下列物质的化学式分别为:甲:_________;丙:____________; 丁:____________。
(2)戊的电子式为____________。
(3)写出白色沉淀A与乙反应的离子方程式:_________________。
Ⅱ.(4)已知工业制备二甲醚的催化反应室中进行下列反应:
CO(g)+2H2(g)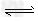 ?CH3OH(g)?△H=-90.7?kJ/mol?①
?CH3OH(g)?△H=-90.7?kJ/mol?①
2CH3OH(g)?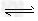 CH3OCH3(g)+H2O(g) △H=-23.5?kJ/mol②
CH3OCH3(g)+H2O(g) △H=-23.5?kJ/mol②
CO(g)+H2O(g)?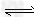 CO2(g)+H2?(g) △H=-41.2?kJ/mol③
CO2(g)+H2?(g) △H=-41.2?kJ/mol③
则催化反应室中总反应3CO(g)+3H2?(g)?CH3OCH3(g)+ CO2(g)的△H=______________。
参考答案:I.?(1)BaCl2?;Ba(NO3)2?;Na2SO4 ?
(2)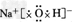
(3)BaCO3+2H+=Ba2+ +CO2↑+H2O
Ⅱ(4)-246.1?kJ/mol
本题解析:
本题难度:一般
4、选择题 以下是对某水溶液进行离子检验的方法和结论,其中正确的是( )
A.先加入BaCl2溶液,再加入足量的HNO3溶液,产生了白色沉淀,则溶液中一定含有SO42-
B.用洁净的铂丝蘸取待测液置于酒精灯外焰灼烧时,焰色反应为黄色,则说明存在Na+
C.加入足量的HCl溶液,有气体产生,将气体通入澄清石灰水有白色沉淀,则溶液中一定含有CO32-
D.加入足量浓?NaOH溶液,产生了带有强烈刺激性气味的气体且该气体可以使湿润的红色石蕊试纸变蓝,则溶液中一定含有NH4+
参考答案:A.先加入BaCl2溶液,可能生成AgCl沉淀,并且加入硝酸,也不能排除SO32-的干扰,故A错误;
B.钠的焰色反应为黄色,待测液置于酒精灯外焰灼烧时,焰色反应为黄色,一定含有钠元素,说明溶液中含有Na+,故B正确;
C.溶液中可能含有HCO3-、CO32-等离子,故C错误;
D.能在碱性条件下反应生成具有碱性的气体为NH3,说明溶液中一定含有NH4+,故D正确.
故选BD.
本题解析:
本题难度:简单
5、填空题 醛类因易被氧化为羧酸,而易使酸性高锰酸钾溶液或溴水褪色。向乙醛中滴入酸性KMnO4溶液,可观察到的现象是__________。现已知柠檬醛的结构式为 ,若要检验其中的碳碳双键,其实验方法是_______________。
参考答案:酸性KMnO4溶液褪色? ;
先取少量柠檬醛溶液于一试 管中,再加入足量银氨溶液,水浴加热。反应后取上层清液,然后再加少量酸性KMnO4溶液,振荡。若酸性KMnO4溶液褪色,则证明该分子中有C=C键存在,否则不存在C=C键
本题解析:
本题难度:一般