1、填空题 I.短周期元素X、Y、Z、W在元素周期表中相对位置如图所示,其中Y所处的周期序数与族序数相等。按要求回答下列问题:
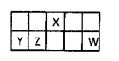
(1)写出X的原子结构示意图_______________。
(2)列举一个事实说明W非金属性强于Z: _______________(用化学方程式表示)。
(3)含Y的某种盐常用作净水剂,其净水原理是__________(用离子方程式表示)。
II.运用所学化学原理,解决下列问题:
(4)已知:Si+2NaOH+H2O=Na2SiO3+2H2。某同学利用单质硅和铁为电极材料设计原电池(NaOH为电解质溶液),该原电池负极的电极反应式为_________________。
(5)已知:①C(s)+ O2(g)=CO2(g)?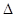 H=a kJ・ mol-1;②CO2(g) +C(s)=2CO(g)
H=a kJ・ mol-1;②CO2(g) +C(s)=2CO(g) 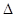 H=b kJ・ mol-1;③Si(s)+ O2(g)=SiO2(s)?
H=b kJ・ mol-1;③Si(s)+ O2(g)=SiO2(s)?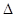 H=c kJ・ mol-1。工业上生产粗硅的热化学方程式为____________。
H=c kJ・ mol-1。工业上生产粗硅的热化学方程式为____________。
(6)已知:CO(g)+H2O(g) H2(g) + CO2(g)。右表为该反应在不同温度时的平衡常数。则:该反应的
H2(g) + CO2(g)。右表为该反应在不同温度时的平衡常数。则:该反应的 H________0(填“<”或“>”);500℃时进行该反应,且CO和H2O起始浓度相等,CO平衡转化率为_________。
H________0(填“<”或“>”);500℃时进行该反应,且CO和H2O起始浓度相等,CO平衡转化率为_________。
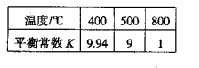
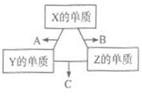
2、选择题 X、Y、Z三种短周期元素,其单质在常温下均为无色气体,它们的原子序数之和为16。在适当条件下三种单质两两化合,可发生如图所示变化。己知1个B分子中含有Z元素的原子个数比C分子中含有Z元素的原子个数少1个。下面判断正确的是
A.原子半径:Z<Y<X
B.非金属性:Z>Y>X
C.化合物A易溶于水
D.化合物B与C的混合物呈碱性
3、填空题 (14分)下表列出了前三周期部分元素在周期表中的位置。请根据表中信息回答下列问题:
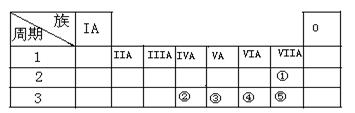
(1)②的元素符号为?
(2)③、④、⑤中原子半径最大的是??(填元素符号)。
(3)Mg与⑤两种元素形成的化合物为??化合物(填“离子”或“共价”)。?
(4)上表中非金属性最强的是??(填元素名称)请用元素周期律的知识说明原因?
?
(5)②③④⑤这四种元素的气态氢化物中稳定性最小的是??最高价氧化物对应水化物中酸性最强的是??(填分子式)
4、选择题 已知:元素X的电负性数值为2.5,元素Y的电负性数值是3.5,元素Z的电负性数值为1.2,元素W的电负性数值为2.4。你认为上述四种元素中,哪两种最容易形成离子化合物(?)
A.X与Y
B.X与W
C.Y与Z
D.Y与W
5、选择题 现有一瓶A和B的混合物,已知它们的性质如下表。
A.过滤
B.蒸发
C.分液
D.蒸馏