1、填空题 (1)工业上制取纯硅涉及以下三个反应:
①SiO2+2C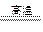 Si(粗)+2CO↑? ②Si(粗)+2Cl2
Si(粗)+2CO↑? ②Si(粗)+2Cl2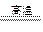 SiCl4
SiCl4
③SiCl4+2H2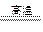 Si(纯)+4HCl
Si(纯)+4HCl
其中属于置换反应的有___?_;反应①、②、③的反应物中有C、H2、Cl2、SiO2,按照某种物质分类标准,它们中有一种物质与其他三种物质明显不同,该物质为?,写出分类的依据??(只需写出一种分类方法)。
(2)碳、铝均能还原铁的氧化物。为确定混合物(含FeO、Fe2O3)的组成,现进行如下实验:
①取一定质量混合物与足量炭粉共热,只收集到CO气体m mol;
②取与①相同质量的混合物与足量铝进行铝热法炼铁,得到单质铁n mol则混合物中FeO的物质的量分数是?(用m、n表示)。
③经测定,消耗1mol碳粉还原固体Fe2O3生成固体铁和CO气体,放出akJ热量,请写出该反应的热化学方程式?。
参考答案:(1)①③? SiO2(2分)? SiO2为氧化物?(2分)
(2)②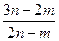 ×100%?(3分)
×100%?(3分)
③Fe2O3(s)+3C(s)=2Fe(s)+3CO(g)?△H=―3akJ・mol-1
本题解析:略
本题难度:简单
2、选择题
A.Na2O2和CO2
B.Na和O2
C.NaOH和CO2
D.C和O2
参考答案:A
本题解析:Na与O2反应时,若暴露在空气中不加热则生成氧化钠,加热或点燃则生成过氧化钠;NaOH和CO2反应时,会因二氧化碳的多少而生成碳酸钠或碳酸氢钠;C和O2反应则会因氧气的量不同而生成二氧化碳或一氧化碳。
本题难度:简单
3、选择题 下列物质不能用玻璃器皿贮存的是
A.苛性钠
B.氢氟酸
C.浓硫酸
D.硝酸铵
参考答案:B
本题解析:不能用玻璃器皿,是常温下要和玻璃反应的物质.玻璃是以含硅物质为原料,经加热制成的硅酸盐产品,普通玻璃是硅酸钠(Na2SiO3)、硅酸钙(CaSiO3)和二氧化硅(SiO2)熔化在一起所得到的物质,二氧化硅是酸性氧化物,不溶于水,能跟碱性氧化物或碱发生反应生成盐,苛性钠是氢氧化钠的俗名,玻璃中含的二氧化硅能够被碱腐蚀.SiO2+2NaOH=Na2SiO3+H2O,实验室里盛放碱溶液的试剂瓶常用橡胶塞,而不用玻璃塞,因为玻璃塞是磨口的,表面积大,以防止玻璃与碱反应生成Na2SiO3而把瓶口和塞子粘结在一起,排除A;氢氟酸遇二氧化硅很快反应放出氟化硅气体: SiO2(固)+4HF=SiF4↑+2H2O。玻璃瓶不能盛放氢氟酸,通常氢氟酸盛放在塑料瓶中,B对;浓硫酸和硝酸铵跟玻璃都不反应,可以贮存。
本题难度:简单
4、选择题 下列有关说法正确的是
A.太阳能电池板中的硅在元素周期表中处于金属与非金属的交界位置
B.天然气、沼气和水煤气均属于可再生能源
C.硫酸、纯碱、醋酸钠分别属于酸、碱、盐
D.生铁、普通钢和不锈钢中的碳含量依次增加
参考答案:A
本题解析:略
本题难度:简单
5、选择题
A.NH4HCO3
B.K2CO3
C.Ca(HCO3)2
D.KClO3
参考答案:C
本题解析:NH4HCO3受热分解无残渣剩余,K2CO3受热不分解,KClO3受热分解放出氧气并得到残渣氯化钾,氯化钾与盐酸则不反应。
本题难度:简单