1������� ���ո���ɣ����ֶ�����Ԫ�ص����ʻ�ṹ��Ϣ���±����������Ϣ�ش��������⣮
| Ԫ�� | A | B | C | D
���ʻ�
�ṹ
��Ϣ
�����µ���Ϊ��ɫ��ĩ״���壬�������ۻ���������������ȼ�գ���������������ɫ���棬�����д̼�����ζ������
���ʳ��¡���ѹ�������壬������ˮ��ԭ�ӵ�M������7������
��������������ɫ���塢������ǿ�������ڿ�����ȼ�շ�����ɫ�Ļ��棬���ɵ���ɫ�Ĺ���
ԭ��������Ӳ���4�����ӣ��䵥�ʼ������ᷴӦ��������Ӧ
|
��1��BԪ�������ڱ��е�λ����______��д��C������ȼ�պ����ĵ���ʽ______��
��2��д��C������ˮ��Ӧ�Ļ�ѧ����ʽ______��A����Ԫ���γɵĻ���������ˮ����Һ��pH______7������ڡ������ڡ���С�ڡ�����
��3��D���ᷴӦ�Ļ�ѧ����ʽΪ______��NaOH��Ӧ�����ӷ���ʽΪ______��
��4��A��B��Ԫ�طǽ����Խ�ǿ���ǣ�дԪ�ط��ţ�______��д��������������Ӧˮ���������ǿ��______�����û�ѧʽ��ʾ��
�ο��𰸣�Ԫ��A����������Ϊ��ɫ��ĩ״���壬�������ۻ���������������ȼ�գ���������������ɫ���棬�����д̼�����ζ�����壬����AΪSԪ�أ�
Ԫ��Bԭ�ӵ�M������7�����ӣ��ҵ��ʳ��¡���ѹ�������壬������ˮ������B��ClԪ�أ�
CԪ�ص����ڿ�����ȼ�շ�����ɫ�Ļ��棬���ɵ���ɫ�Ĺ��壬��������������ɫ���塢������ǿ������CΪNaԪ�أ�
DԪ��ԭ��������Ӳ���4�����ӣ����Ƕ�����Ԫ�أ�DԪ��Ϊ��AԪ�أ���CԪ�ػ�SiԪ�أ�̼����Ũ���ᡢŨ���ᷴӦ����������Ӧ��������HF�ᷴӦ��Ҳ����NaOH��Ӧ�������䵥�ʼ������ᷴӦ��������Ӧ������ΪSiԪ�أ�
��1��B��ClԪ�أ�ԭ�ӽṹʾ��ͼΪ

�����Ӳ���=������������������=�����������������ǵ������ڵڢ�A��Ԫ�أ�Na������ȼ�պ����ΪNa2O2������ʽ��
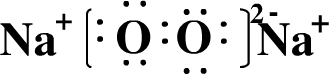
���ʴ�Ϊ���������ڵڵڢ�A�壻
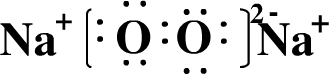
��
��2��C���ƣ���ˮ��Ӧ�ķ���ʽΪ��2Na+2H2O=2NaOH+H2����A��������Ԫ���γɵĻ�������H2S������ˮ����Һ�����ԣ�����pH��7��
�ʴ�Ϊ��2Na+2H2O=2NaOH+H2����С�ڣ�
��3��D��Si������HF��Ӧ����Ӧ����ʽΪ��Si+4HF�TSiF4��+2H2����Si��ǿ�Ӧ�����κ��������������ӷ���ʽΪ��Si+2OH-+H2O=SiO32-+2H2����
�ʴ�Ϊ��Si+4HF�TSiF4��+2H2����Si+2OH-+H2O=SiO32-+2H2����
��4��A��SԪ�أ�B��ClԪ�أ�����Ԫ��������֪����Ԫ�طǽ����Դ�����Ԫ�أ�
A��B��Ԫ������������Ӧˮ�������ֱ���H2SO4��HClO4��HClO4�����ԣ�H2SO4�����ԣ�
�ʴ�Ϊ��Cl��HClO4�����ԣ�H2SO4�����ԣ�
���������
�����Ѷȣ�һ��
2��ѡ���� ���з�Ӧ�����ӷ���ʽ��ȷ����?��?��
A����FeCl3��Һ��ͭ��Ӧ����ӡˢ��·�壺Cu+Fe3+===Cu2++Fe2+
B��̼����þ��Һ�м������ʯ��ˮ��
 Mg2++2HCO3��+Ca2++2OH��====CaCO3��+2H2O+MgCO3��
Mg2++2HCO3��+Ca2++2OH��====CaCO3��+2H2O+MgCO3��
C���ö��Ե缫���MgCl2��Һ��2Cl��+2H2O 2OH��+Cl2��+H2��
D���ں���Mn2+����Һ�м���HNO3?���ټ���PbO2����Ӧ����Һ���Ϻ�ɫ��