1、选择题 能正确表示下列反应的离子方程式是

A.向次氯酸钙溶液通入过量CO2:Ca2++2ClO-+CO2+H2O =CaCO3↓+2HClO

B.向次氯酸钙溶液通入SO2:Ca2++2ClO-+SO2+H2O= CaSO3↓+2HClO

C.氢氧化钙溶液与碳酸氢镁溶液反应:HCO3-+Ca2++OH-=CaCO3↓+H2O

D.在氯化亚铁溶液中加入稀硝酸:3Fe2++4H++NO3-=3Fe3++NO↑+2H2O
参考答案:D
本题解析:A选项CO2过量的话,应该生成HCO3-方程式应为:ClO-+CO2+H2O=HClO+HCO3-;B选项HClO可将CaSO3氧化为CaSO4,正确的方程式为:Ca2++ClO-+SO2+H2O=CaSO4↓+Cl-+2H+;C选项要考虑到Mg(OH)2为沉淀即可, Mg2++2HCO3-+2Ca2++4OH-=Mg(OH)2↓+2CaCO3↓+2H2O。
本题难度:一般
2、选择题 下列反应的离子方程式书写正确的是?(?)
A.AgNO3溶液中加入过量氨水:Ag++NH3・H2O=AgOH↓+NH4+
B.溴化亚铁溶液中通人少量氯气:2Fe22++C12=2Fe3++2Cl-
C.碳酸钙溶于过量的甲酸:CaCO3+2H+=Ca2++CO2↑+H2O
D.澄清石灰水与少量苏打溶液混合:Ca2++OH-+HCO3-=CaCO3↓+H2O
参考答案:B
本题解析:略
本题难度:简单
3、选择题 下列离子方程式书写正确的是(? )
A.在蓝色的淀粉溶液中通入足量SO2后成无色溶液:I2+SO2+2H2O=2I-+SO32-+4H+
B.等物质的量的亚硫酸氢铵与氢氧化钠溶液混合:NH4++HSO3-+2OH-=SO32-+NH3↑+2H2O
C.碳酸氢镁溶液中加入过量石灰水:Mg2++2HCO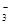 +Ca2++2OH-=CaCO3↓+2H2O+MgCO3↓
+Ca2++2OH-=CaCO3↓+2H2O+MgCO3↓
D.碳酸氢钠溶液中加入过量氢氧化钡溶液:HCO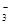 +Ba2++OH-=BaCO3↓+H2O
+Ba2++OH-=BaCO3↓+H2O
参考答案:D
本题解析:碘单质具有氧化性,能把SO2氧化生成硫酸,方程式为I2+SO2+2H2O=2I-+SO42-+4H+。B中氢氧化钠不足,生成物应是亚硫酸钠和亚硫酸铵,方程式为HSO3-+OH-=SO32- +2H2O。氢氧化镁比碳酸镁的溶解度小,所以C中生成物是氢氧化镁,方程式为Mg2++HCO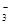 +Ca2++3OH-=CaCO3↓+H2O+Mg(OH)2↓。所以正确的答案是D。
+Ca2++3OH-=CaCO3↓+H2O+Mg(OH)2↓。所以正确的答案是D。
本题难度:一般
4、选择题 下列离子方程式改写成的化学方程式正确的是
[? ]
A. Cu2++2OH-=Cu(OH)2↓ CuCO3+2NaOH=Cu(OH)2↓+Na2CO3
B. CO32-+2H+=CO2↑+H2O BaCO3+2HCl=BaCl2+CO2↑+H2O
C. Ca2++CO32-=CaCO3↓ Ca(NO3)2+Na2CO3=CaCO3↓+2NaNO3
D. H++OH-=H2O Ba(OH)2+H2SO4=BaSO4↓+2H2O
参考答案:C
本题解析:
本题难度:简单
5、填空题 以冶铝的废弃物铝灰为原料制取超细α-氧化铝,既降低环境污染又可提高铝资源的利用率。已知铝灰的主要成分为Al2O3(含少量杂质SiO2、FeO、Fe2O3),其制备实验流程如下:
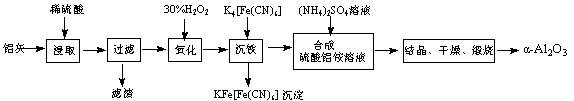
(1)铝灰中氧化铝与硫酸反应的化学方程式为?。
(2)图中“滤渣”的主要成分为??(填化学式)。
(3)加30%的H2O2溶液发生的离子反应方程式为?。
(4)煅烧硫酸铝铵晶体,发生的主要反应为:
4[NH4Al(SO4)2・12H2O]  2Al2O3 + 2NH3↑+ N2↑+ 5SO3↑+ 3SO2↑+ 53H2O,将产生的气体通过下图所示的装置。
2Al2O3 + 2NH3↑+ N2↑+ 5SO3↑+ 3SO2↑+ 53H2O,将产生的气体通过下图所示的装置。
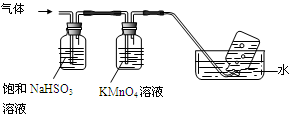
①集气瓶中收集到的气体是??(填化学式)。
②足量饱和NaHSO3溶液吸收的物质除大部分H2O(g)外还有??(填化学式)。
③KMnO4溶液褪色(MnO4-还原为Mn2+),发生的离子反应方程式为?。
参考答案:
(1)Al2O3 + 3H2SO4 = Al2(SO4)3 + 3H2O(2分)
(2)SiO2(2分)
(3)2Fe2++H2O2+2H+ = 2Fe3++2H2O(2分)
(4)①N2(2分)②SO3、NH3(2分,缺漏不给分)。
③2MnO4- +5SO2 + 2H2O = 2Mn2+ + 5SO42-+4H+(2分)
本题解析:(1)氧化铝为两性氧化物与酸、碱均反应;(2)铁的氧化物和氧化铝溶于酸,二氧化硅不溶形成滤渣;(3)溶液中的亚铁离子不易除去,需把其氧化为铁离子再沉淀除去;(4)①通过饱和亚硫酸氢钠溶液除去氨气、三氧化硫,通过高锰酸钾溶液除去二氧化硫气体,故收集的气体为氮气;②SO3、NH3均溶解于水与水反应;③KMnO4溶液与二氧化硫反应,二氧化硫被氧化为硫酸根离子。
本题难度:一般