1、选择题 空气和CO2按体积比5∶1混合,将混合气体与足量的红热焦炭充分反应,设空气中N2和O2的体积比为4∶1,不计其他成分,且体积均在同温、同压下设定,则反应后的气体中CO的体积分数是?
A.50%
B.29%
C.43%
D.100%
参考答案:A
本题解析:
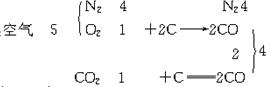 ?
?
则CO%=50%。
答案:A
本题难度:简单
2、选择题 下列说法正确的是
A.1 mol O2和1 mol N2所占有的体积都约是22.4L
B.H2的气体摩尔体积约为22.4L
C.在标准状况下,1 mol H2和1mol H2O所占的体积都约是22.4L
D.在标准状况下,22.4L由N2和N2O组成的混合气体中,所含有的氮原子的物质的量2mol
参考答案:D
本题解析:略
本题难度:简单
3、选择题 已知2.16 gX2O5中含有0.1 mol氧原子,则X的相对原子质量为? ( )
?
A.28
B.28g/mol
C.14
D.14g/mol
参考答案:C
本题解析:2.16 gX2O5中含有0.1 mol氧原子,即2.16 gX2O5的物质的量为0.02mol,由关系式得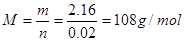 ,即相对分子质量为108,所以得X的相对原子质量为14;
,即相对分子质量为108,所以得X的相对原子质量为14;
本题难度:一般
4、填空题 (1)由三个原子构成的某气体分子,其摩尔质量为M g/mol,该气体的体积为V L(标准
状况),设阿伏加德罗常数的值为NA,则:
①该气体的物质的量为________mol;
②该气体中所含的原子总数为________个;
③该气体在标准状况下的密度为________g/L;
④该气体的一个分子的质量为________g。
(2)气体化合物A分子式可表示为OxFy,已知同温同压下10 mL A受热分解生成15 mL O2和10 mL F2,则A的化学式为________,推断的依据为______________________
________________________________________________________________________。
参考答案:(1)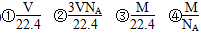
(2)O3F2 阿伏加德罗定律和质量守恒定律
本题解析:(1)由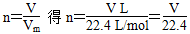 mol,含有分子数为
mol,含有分子数为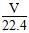 NA,原子数为分子数的3倍:
NA,原子数为分子数的3倍: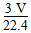 NA;密度是单位体积气体的质量:
NA;密度是单位体积气体的质量: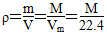 g/L;1 mol气体中含有NA个分子,一个分子的质量为
g/L;1 mol气体中含有NA个分子,一个分子的质量为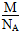 g。
g。
(2)根据质量守恒定律和阿伏加德罗定律,写出分解方程式为2OxFy ?3O2+2F2,则A的化学式为O3F2。
?3O2+2F2,则A的化学式为O3F2。
本题难度:一般
5、选择题 用NA表示阿伏加德罗常数的值。下列说法错误的是
A.1mol Na作为还原剂时可提供的电子数为NA
B.标准状况下,22.4L氯气中所含的氯原子数为2NA
C.0.5mol/L的MgCl2溶液中,含有Cl-个数为NA
D.18g水中所含的电子数为10NA
参考答案:C
本题解析:A 对 钠化合价由0价升高到+1价,失去1mol电子
B 对 标况下,22.4L氯气为1mol,含的氯原子数为2NA
C 错没有给溶液体积,无法求Cl-个数
D 对18g水为1mol,含电子数为10NA
本题难度:一般