1、填空题 物质在制取或配制成溶液时往往应用化学平衡的知识.
(1)钾是一种活泼的金属,工业上通常用金属钠和氯化钾在高温下反应制取.该反应为:Na(l)+KCl(l) ?NaCl(l)+K(g) ΔH>0,该反应的平衡常数可表示为:K=c(K),各物质的沸点与压强的关系见下表.
?NaCl(l)+K(g) ΔH>0,该反应的平衡常数可表示为:K=c(K),各物质的沸点与压强的关系见下表.
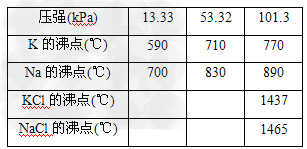
①在常压下金属钾转变为气态从反应混合物中分离的最低温度约为________,而反应的最高温度应低于________.
②常压下,当反应温度升至900℃时,该反应的平衡常数可表示为:K=________.
(2)实验室中配制碘水,往往是将I2溶于KI溶液中,这样就可以得到浓度较大的碘水,主要是因为发生了反应:I2(aq)+I- ?I3- 上述平衡体系中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上的任何一点都表示平衡状态).
?I3- 上述平衡体系中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上的任何一点都表示平衡状态).
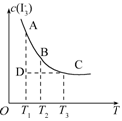
①通过分析上图,该反应的正反应为________反应(填“吸热”或“放热”).
②在T1、D状态时,v正________v逆(填“>”“<”或“=”).
2、选择题 下图表示可逆反应mA(g)+nB(g)? pC(g)在不同温度(T)、压强(p)下,生成物C的物质的量分数x(C)的变化情况.下列关于该正反应热效应及方程式中A、B、C的化学计量数的判断中,正确的是
pC(g)在不同温度(T)、压强(p)下,生成物C的物质的量分数x(C)的变化情况.下列关于该正反应热效应及方程式中A、B、C的化学计量数的判断中,正确的是
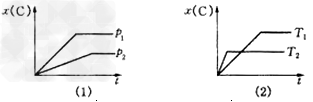
[? ]
A.放热反应,m+n>p
B.吸热反应,m+n>p
C.放热反应,m+n<p
D.吸热反应,m+n=p
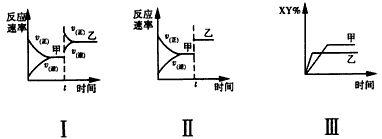
3、选择题 在密闭容器中,反应X2(g)+Y2(g)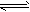 2XY(g) △H<0,达到甲平衡。下面的三个图形表示了在仅改变某一条件后,达到乙平衡的情况,对此过程的分析正确的是
2XY(g) △H<0,达到甲平衡。下面的三个图形表示了在仅改变某一条件后,达到乙平衡的情况,对此过程的分析正确的是
[? ]
A.图I是加入适当催化剂的变化情况
B.图Ⅱ是扩大容器体积的变化情况
C.图Ⅲ是增大压强的变化情况
D.图Ⅲ是升高温度的变化情况
4、填空题 在A+B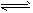 2C的反应中,在某温度下经t s后混合物中C 的百分含量的变化情况如图所示。则
2C的反应中,在某温度下经t s后混合物中C 的百分含量的变化情况如图所示。则
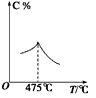
(1)A与B化合生成C的反应是_________热反应。
(2)温度在475℃以下,随温度升高,C的百分含量增大,这是因为_________________________。
(3)当温度在475℃以上,随温度升高,C的百分含量反而减小,这是因为_____________________。
(4)当温度在475℃时,若B为气态,体系加压时,C的浓度不变,则A、C的状态又如何?
___________________________。
5、选择题 对已达平衡的下列反应 2X(g)+Y(g) 2Z(g),减小压强时,对反应产生的影响是
2Z(g),减小压强时,对反应产生的影响是
[? ]
A.逆反应速率增大,正反应速率减小,平衡向逆反应方向移动
B.逆反应速率减小,正反应速率增大,平衡向正反应方向移动
C.正、逆反应速率都减小,平衡向逆反应方向移动
D.正、逆反应速率都增大,平衡向正反应方向移动