1��ѡ���� LiFePO4��ؾ����ȶ��Ըߡ���ȫ���������ŵ㣬�����ڵ綯��������ط�ӦΪ��
FePO4+Li 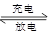 LiFePO4����ص�����������LiFePO4������������ʯī����Li���������Ϊ����ʡ������й�LiFePO4���˵���������
LiFePO4����ص�����������LiFePO4������������ʯī����Li���������Ϊ����ʡ������й�LiFePO4���˵���������
A���ɼ�����������ߵ���ʵĵ�����
B���ŵ�ʱ����ڲ�Li���������ƶ�
C���������У�����������ϵ���������
D���ŵ�ʱ���������ӦΪ��FePO4+Li++e-=LiFePO4
�ο��𰸣�A
����������������֪���õ�صĵ����Ϊ�������ʣ����Բ��ɼ�����������ߵ���ʵĵ����ԣ���A����Ϊ����Ĵ𰸣��ɵ�ط�ӦFePO4+Li 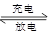 LiFePO4����֪�����ŵ�ʱ����ڲ�Li���������ƶ�����B��ȷ���������У�����������ϵ��������٣���C��ȷ���ŵ�ʱ���������ӦΪ��FePO4+Li++e-=LiFePO4����D��ȷ��
LiFePO4����֪�����ŵ�ʱ����ڲ�Li���������ƶ�����B��ȷ���������У�����������ϵ��������٣���C��ȷ���ŵ�ʱ���������ӦΪ��FePO4+Li++e-=LiFePO4����D��ȷ��
���������⿼���˽��ԭ��ص�֪ʶ������LiFePO4��أ����ߣ�ע�Ȿ��Ҫ���úñ������ɵ���Ϣ��������һ�����Ѷȡ�
�����Ѷȣ�һ��
2��ѡ���� Ϊ�˱�����ͭ������ͭ�̣����·�����ȷ����
[? ]
A������ͭ����������������
B������ͭ����ֱ����Դ����������
C������ͭ�������ڳ�ʪ�Ŀ�����
D������ͭ���ı��渲��һ������ĸ߷���Ĥ
�ο��𰸣�D
���������
�����Ѷȣ���
3������� ��ͼ��aΪ������A�ձ��з��뱽��B�ձ���Ϊ1 mol��L��1��ϡ���ᣬC�ձ���Ϊ��ˮ��
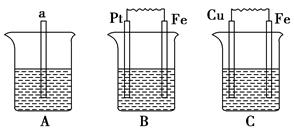
(1)B��Pt���ĵ缫��ӦʽΪ________��
(2)C��Cu���ĵ缫��ӦʽΪ________��Cu��������Һ��pH________(���������С�����䡱)��
(3)�Ƚ�A��B��C��������ʴ�����ʣ��ɿ쵽����˳����________��
(4)ҪʹB�е����ѱ���ʴ���ɽ�B�е�ϡ�����Ϊ________��
�ο��𰸣�(1)2H����2e��=H2��
(2)2H2O��O2��4e��=4OH��������
(3)B>C>A
(4)�ƾ�(�����Ȼ�̼��)
���������(1)B��Pt���ĵ缫��ӦʽΪ2H����2e��=H2����(2)C��Cu����������������ԭ��Ӧ���缫��ӦʽΪ2H2O��O2��4e��=4OH����Cu��������Һ��pH����(3)����Fe��Pt�Ļ�Բ���Fe��Cu��B�з�Ӧ���ʿ죬��A�������DZ��������ױ���ʴ���ʸ�ʴ�����ɿ쵽����˳����B>C>A��(4)ҪʹB�е����ѱ���ʴ���ɽ�B�е�ϡ�����Ϊ�ǵ������Һ����ƾ����������Ȼ�̼�ȡ�
�����Ѷȣ�һ��
4������� ��6�֣�Ϊ�˷�ֹ������ʴ��������Ƥ�������һ�����ʴ�Ľ��������п���Ͷ�����������ͷ��װެ�ѽ����ù�ͷ�IJ���Ӧѡ��������?������ȡһС���п��Ƥ�Ͷ�����Ƥ����С��������̻���¶�����������Ȼ���ڿ̺��ϵ�һ���Ȼ�����Һ���ٵ�һ��K3[Fe(CN)6]��Һ��K3[Fe(CN)6]��Һ����Fe2+�������ɫ�����������������Ӻ��ȳ�����ɫ�����������һ����Ƭ??��
����Ƭ�Ϸ����ĵ缫��ӦʽΪ?��
����һ�ֽ����Ϸ����ĵ缫��ӦʽΪ?��
�ο��𰸣���6�֣�
������1�֣���������1�֣���Fe-2e��==Fe2+��2�֣���O2+2H2O+2e��=4OH-��2�֣�
�����������
�����Ѷȣ���
5��ѡ���� ��ѹǿ������̽��������pH=2��pH=4������Һ�з�����ʴ��װ�ü��õ���ͼ�����£�
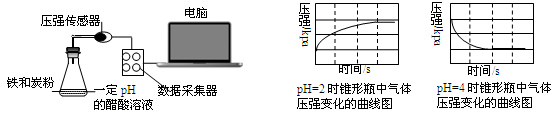
����ͼ�����½��۴������
A����ҺpH��2ʱ�������������ⸯʴ
B����������Һ���������ܷ���������ʴ
C�����ⸯʴ��������ʴ������һ����
D������Һ�и�����Ӧ��Ϊ��Fe �C 2e��Fe2+
�ο��𰸣�C
���������A�������ⸯʴ����������ȷ����ͼ2���Կ�����PH=4ʱѹǿ��С��˵����������������ʴ��B����������Һ���������ܷ���������ʴ����ȷ��C���жϸ�ʴ���ʿ���������D��������������ʧȥ���ӣ���ȷ��
�����Ѷȣ���