1、选择题 下列变化中,需要加入氧化剂才能实现的是:(?)
A.MnO2 →MnSO4
B.CuO→Cu
C.KI →KIO3
D.HNO3→NO
参考答案:C
本题解析:A.转化MnO2→MnSO4中,锰元素化合价降低,需加入还原剂才能实现,故A错误;
B.转化CuO→Cu中,铜元素化合价降低,需加入还原剂才能实现,故B错误;
C.转化KI→KIO3中,碘元素化合价升高,需加入氧化剂才能实现,故C正确;
D.转化HNO3→NO中,氮元素化合价降低,需加入还原剂才能实现,故D错误。
故选C。
点评:本题考查学生氧化还原反应的基本知识,可以根据所学知识进行回答,难度不大。
本题难度:一般
2、选择题 下列物质分别与水的反应中,属于氧化还原反应,但水既不是氧化剂也不是还原剂的是
A.氧化钙
B.铁
C.过氧化钠
D.二氧化硫
参考答案:C
本题解析:A、CaO+H2O=Ca(OH)2;非氧化还原反应
B、3Fe+4H2O(g) Fe3O4+4H2;水做氧化剂;
C、2Na2O2+2H2O=4NaOH+O2↑,水既不是氧化剂也不是还原剂;
D、SO2+H2O=H2SO3;非氧化还原反应
本题难度:简单
3、简答题 0.4g氢氧化钠恰好与10ml的盐酸完全反应,试求这种盐酸的物质的量浓度是多少?
参考答案:NaOH的物质的量为0.4g40g/mol=0.01mol,
由NaOH+HCl=NaCl+H2O
? 1? 1
则HCl的物质的量为0.01mol,
盐酸10mL,则盐酸的浓度为0.01mol0.01L=1mol/L,
答:这种盐酸的物质的量浓度为1mol/L.
本题解析:
本题难度:一般
4、选择题 很多化学物质名称中含有“水”,“水”通常有三种含义:①表示水这种物质;②表示水溶液;③表示物质处于液态。下列物质名称中的“水”不属于以上三种含义的是
A.水晶
B.水银
C.溴水
D.重水
参考答案:A
本题解析:A、水晶只是物质的名称,成分是SiO2,不表示上面的任何一种含义,故A错误;
B、水银是一种液态金属的叫法,表示了汞处于液态,故B正确;
C、溴水是溴的水溶液,故C正确;
D、重水是水中的一种,表示了水这种物质,故D正确。
故选A。
点评:考查学生对物质的理解,比较基础,在解此类题时,首先要对水的三种含义有个全面的认识,然后结合选项中的叙述进行判断。
本题难度:简单
5、选择题 取50mL稀硫酸与一定质量的镁、铝合金反应,合金全部溶解,向所得溶液中滴加5mol?L-1?NaOH溶液到过量,生成沉淀质量与加入NaOH溶液体积关系如图,则( )
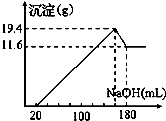
A.原合金中铝质量为7.8g
B.原合金的质量为19.4g
C.原合金中镁的质量为4.8g
D.硫酸的物质的量浓度为5mol?L-1
参考答案:A、氢氧化铝的质量为19.4-11.6=7.8g,故A错误;
B、氢氧化铝和氢氧化铝沉淀的总质量为19.4g,故原合金质量一定小于19.4g,故B错误;
C、氢氧化镁的物质的量等于金属镁的物质的量=11.6g58g/mol×24g/mol=4.8g,故C正确;
D、氢氧化钠溶液加入到溶液至沉淀量最大量时,硫酸全部生成硫酸钠,硫酸物质的量等于氢氧化钠物质的量的12,根据图象可知氢氧化镁物质的量等于镁的物质的量=4.8g24g/mol=0.2mol;氢氧化铝物质的量=7.8g78g/mol=0.1mol,生成这些沉淀共需氢氧化钠物质的量=0.2mol×2+0.1mol×3=0,7mol,需要氢氧化钠的体积为0.7mol5mol/L=0.14L,所以加入氢氧化钠的体积共160ml,此时硫酸根全为硫酸钠,则根据关系;2NaOH~Na2SO4~H2SO4可知 硫酸物质的量=0.16L×52=0.4mol,硫酸的浓度=0.4mol0.05L=8mol/L,故D错误;
故选C.
本题解析:
本题难度:一般