1、选择题 甲、 乙、 丙、 丁四种易溶于水的物质,分别由Na+、Ba2+、Al3+、H+、OH-、Cl-、HCO3-、SO42-中的不同阳离子和阴离子各一种组成,已知:
①0.1 mol/L甲溶液中c(H+)>0.1 mol/L;
②将少量乙溶液分别滴入其他三种物质的溶液时,均有白色沉淀生成;
③向丙溶液中滴入AgNO3溶液有不溶于稀HNO3的白色沉淀生成。?下列判断正确的是
A.甲溶液含有SO42-
B.乙溶液含有SO42-
C.丙溶液显酸性
D.丁溶液显酸性
参考答案:AC
本题解析:①根据0.1mol/L甲溶液中c(H+)>0.1mol/L,可知甲溶液一定是硫酸;②能够和甲(硫酸)反应生成沉淀,说明乙中一定有Ba2+,结合③可知,阴离子只能是OH-或HCO3-;③可以推断丙一定含有Cl-,可能是氯化铝或氯化钠;若是氯化钠,不会和乙生成沉淀,故丙只能是氯化铝,即甲是硫酸,乙是氢氧化钡,丙是氯化铝,丁是碳酸氢钠,因此正确的答案选AC。
本题难度:一般
2、选择题 有五瓶失去标签的溶液,它们分别为:①Ba(NO3)2②KCl ③NaOH ④CuSO4 ⑤Na2SO4如果不用其他任何试剂(包括试纸),用最简便的方法将它们――鉴别开来,则在下列的鉴别顺序中,最合理的是
A.④③①⑤②
B.④①③⑤②
C.①⑤③④②
D.③④①⑤②
参考答案:A
本题解析:略
本题难度:简单
3、选择题 下列关于有机化合物的说法正确的是
A.乙酸和乙酸乙酯可用Na2CO3溶液加以区别
B.戊烷(C5H12)有两种同分异构体
C.乙烯、聚氯乙烯和苯分子均含有碳碳双键
D.糖类、油脂和蛋白质均可发生水解反应
参考答案:A
本题解析:A、乙酸与碳酸钠溶液反应产生气体,乙酸乙酯不与碳酸钠溶液反应,可以鉴别,正确;B、戊烷有3种同分异构体,错误;C、聚乙烯、苯分子中不含有碳碳双键,错误;D、糖类中的单糖不能发生水解反应,错误,答案选A。
本题难度:一般
4、实验题 (12分)某探究小组将一批废弃 的线路板简单处理后,得到含70%Cu、25%Al、4%Fe及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜和硫酸铝晶体的路线:

请回答下列问题:
⑴第①步Cu与酸反应的离子方程式______________ 。
⑵第②步加H2O2的作用是_______________;调溶液pH的目的是使____________生成沉淀。
⑶用第③步所得CuSO4・5H2O制备无水CuSO4的方法是______________。
⑷由滤渣2制取Al2(SO4)3・18H2O ,探究小组设计了三种方案:

上述三种方案中,_______方案不可行,原因是_____________________________;
从原子利用率角度考虑,___________方案更合理。
⑸探究小组用滴定法测定CuSO4・5H2O含量。取a g试样配成100 mL溶液,每次取20.00 mL,消除干扰离子后,用c mol /L?EDTA(H2Y2-)标准溶液滴定至终点,平均消耗EDTA溶液6 mL。滴定反应如下:Cu2+ + H2Y2-= CuY2- + 2H+
写出计算CuSO4・5H2O质量分数的表达式ω= _____________________________ ;
下列操作会导致CuSO4・5H2O含量的测定结果偏高的是_____________。
a.未干燥锥形瓶?
b.滴定终点时滴定管尖嘴中产生气泡?
c.未除净可与EDTA反应的干扰离子
参考答案:(12分)答案:⑴ Cu + 4H+ + 2NO
 Cu2+ + 2NO2↑+ 2H2O?或3Cu + 8H+ + 2NO
Cu2+ + 2NO2↑+ 2H2O?或3Cu + 8H+ + 2NO
 3Cu2+ + 2NO↑+ 4H2O?(2分)
3Cu2+ + 2NO↑+ 4H2O?(2分)
⑵将Fe2+氧化为Fe3+? Fe3+、Al3+
⑶加热脱水
⑷甲?所得产品中含有较多Fe2(SO4)3杂质?乙
⑸ × 100%?(2分)? c?(2分)
本题解析:将金属混合物处理时,(1)铜和浓硝酸、稀硫酸的混合酸:
开始发生:Cu+2NO3-+4H+ Cu2++2NO2↑+2H2O,
Cu2++2NO2↑+2H2O,
最后发生:3Cu+2NO3-+8H+  3Cu2++2NO↑+4H2O;金属混合物中只有Au和Pt不溶于硝酸,其是滤渣的主要成分;
3Cu2++2NO↑+4H2O;金属混合物中只有Au和Pt不溶于硝酸,其是滤渣的主要成分;
(2)第②步加入过氧化氢的目的是将Fe2+氧化为Fe3+;过氧化氢氧化亚铁离子时生成的是铁离子和水,不引入杂质,对环境无污染;调整pH值,使溶液中的Fe3+、Al3+转化为沉淀;
(3)用第③步中所得的五水硫酸铜制取无水硫酸铜的方法是加热脱水;
(4)滤渣2的主要成分是氢氧化铁和氢氧化铝,以此为基础分析该探究小组设计的三种方法,其中方案甲中制得产品中一定含有较多的Fe2(SO4)3杂质;方案乙和丙中,从原子利用的角度考虑,乙方案最合理;
(5)根据探究小组的方案,可知计算五水硫酸铜质量分数的表达式为:
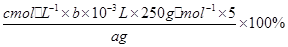 ;
;
滴定过程中,未干燥锥形瓶,对结果无影响,排除a;滴定终点时滴定管尖嘴中产生气泡,造成消耗EDTA的读数偏小,测定结果偏低,排除b;未除净干扰离子,造成EDTA消耗偏多,测定结果偏高,选c。
本题难度:一般
5、选择题 下列关于等质量的SO2和SO3说法,正确的是
A.所含氧原子的个数比为2∶3
B.所含硫原子个数比为1∶1
C.所含硫元素的质量比为5∶4
D.所含原子个数比为3∶4
参考答案:C
本题解析:可用设“1”解题法.先求出二者的物质的量之比,在此基础上推导其他选项.
本题难度:一般