1������� �����ƣ��ѱ��������������ռ�һ����CO2���������������������Һ�������ѿڷ�գ����Է����������������죬������ˣ���һ������������ֻ����첢�������������ӷ�Ӧ����ʽ����ԭ��______��______��______��
�ο��𰸣�CO2�ܺ��������Ʒ�����Ӧ��CO2�����գ�ʹ��������ѹǿ��С����������ѹѹ��������������������Һ��Ӧ����ƫ�����ƺ�ˮ���������ܺ�ǿ�Ӧ�������������¹�������ѹǿ����������¹��𣬶�����̼���������Ʒ�Ӧ��ʵ���ǣ�2OH-+CO2�TCO32-+H2O��������������������Һ��Ӧ����ƫ�����ƺ�ˮ����Ӧ�����ӷ���ʽΪAl2O3+2OH-�T2AlO2-+H2O���������ܺ�ǿ�Ӧ��ʵ���ǣ�2Al+2OH-+2H2O�T2AlO2-+3H2����
�ʴ�Ϊ��CO2+2OH-�TCO32-+H2O��Al2O3+2OH-�T2AlO2-+H2O��2Al+2OH-+2H2O�T2AlO2-+3H2����
���������
�����Ѷȣ�һ��
2������� ��.ͭ�����仯�������ճ�������Ӧ�ù㷺��ij�о���ѧϰС���ô�ͭ��������Fe�������������Ӧ�ù���A����ϡ�����ܽ�A��Ȼ����Լ�������Һ��pH�����ҺB����ҺB��ϵ�в����ɵ��Ȼ�ͭ���壬��ش�
��1������A��ϡ�����ܽ��ԭ����?__��
��2��������ҺB���Ƿ����Fe3���ķ�����?__��
��3����֪Ԫ���ڸ�̬ʱ�����������ԣ���������CuSO4��Һ�м���һ������Na2SO3��NaCl��Һ�����ȣ�����CuCl������������CuCl�����ӷ���ʽ��?��
��.�����£�ijͬѧ��ϡ����Ͱ�ˮ�������ϣ�������Һ��Ũ�Ⱥͻ�Ϻ�������Һ��pH���±���
ʵ����
| ��ˮ���ʵ���Ũ��/��mol��L��1��
| �������ʵ���Ũ��/��mol��L��1��
| �����ҺpH
|
��
| 0.1
| 0.1
| pH��5
|
��
| c
| 0.2
| pH��7
|
��
| 0.2
| 0.1
| pH>7
|
?
��ش�
��4���ӵڢ�������������������û����Һ����ˮ�������c��H������?__mol��L��1���ӵڢ������������c?__���>����<��������0.2 mol��L��1���ӵڢ������������֪�������Һ��c��NH4+��?__���>����<��������c��NH3��H2O����
��5��д������������ҺNH4+Ũ���ɴ�С��˳��?__>?__>?__>?__����ѡ���ţ���
A��0.1 mol��L��1 NH4Cl
B��0.1 mol��L��1 NH4Cl��0.1 mol��L��1 NH3��H2O
C��0.1 mol��L��1 NH3��H2O
D��0.1 mol��L��1 NH4Cl��0.1 mol��L��1 HCl
�ο��𰸣���.��1����ֹ���Ρ�ͭ�η���ˮ�ⷴӦ
��2��ȡ������ҺB���μӼ���KSCN��Һ������������������Һ����Fe3��������Һ���ɫ�������Fe3��
��3��2Cu2����SO32-��2Cl����H2O 2CuCl����SO42-��2H��
2CuCl����SO42-��2H��
��4��1��10��5��������
��5��B��D��A��C
�����������3��CuSO4��Һ�м���һ������Na2SO3��NaCl��������CuCl����������Ԫ�صĻ��ϼ۱仯��֪��SO32-�ᱻ����ΪSO42-����4�������У���ˮ������ǡ�÷�Ӧ�����ɵ��Ȼ�立���ˮ�ⷴӦ���ٽ���ˮ�ĵ��룬��ˮ�������c��H������1��10��5 mol��L��1���ڢ���������Һ�����ԣ�����Ũ�Ȼ�ϣ�����Һ�����ԣ����������ԣ���Ӧ���Ǽ��Թ���������ˮ��Ũ�ȴ���0.2 mol��L��1�����ݼ���ɵã���Ϻ�������Һ�к��е�Ũ�ȵ�NH3��H2O���Ȼ�泥�����pH>7�����Ȼ�淋�ˮ��̶�С��NH3��H2O�ĵ���̶ȣ���c��NH4+��>c��NH3��H2O������5���Ȼ����ǿ����ʣ���ȫ���룬��NH3��H2O��������ʣ����ֵ��룬��C�е�c��NH4+����С����B��ͬʱ�����Ȼ�狀�NH3��H2O���Ҹû����Һ��NH3��H2O�ĵ�������Ȼ�淋�ˮ�⣬��B�е�c��NH4+�����D�д��ڵ��Ȼ���������NH4+��ˮ�⣬��A�е�c��NH4+��С��D�еģ�����c��NH4+���Ĵ�С��ϵ��B>D>A>C��
�㲦�����⿼������ͭ���仯��������ʡ�����Ũ�ȵıȽϣ����鿼�������������������ѶȽϴ�
�����Ѷȣ�����
3��ѡ���� �������ӷ���ʽ��д��ȷ����(? )
A��ʵ������Fe��ϡ������������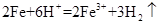
B����Ũ������Mn02��Ӧ��ȡ����������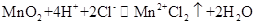
C����̼��������Һ�м����������ƣ�
D��������������Һ��ȥ�����������Ĥ��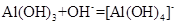
�ο��𰸣�B
���������
��ȷ�𰸣�B
A��Fe��2H�� =Fe2����H2��
C��HCO3�D��OH�D=CO32�D��H2O
D��Al2O3��2OH�D=2AlO2�D��H2O
�����Ѷȣ�һ��
4��ѡ���� �������ӷ���ʽ�У���ȷ����
[? ]
A���Ȼ�������Һ�м������2Fe2+��4H+��NO3-== 2Fe3+��2H2O��NO��
B����AlCl3��Һ�м��������NaOH��Һ��Al3+ + 3OH- == Al(OH)3��
C������������ˮ��Ӧ��3NO2+ H2O == NO+2H+ +2NO3-
D��������������������Һ��Ӧ��Al2O3+2OH- == 2AlO2- + H2O
�ο��𰸣�CD
���������
�����Ѷȣ�һ��
5��ѡ���� �������ӷ���ʽ��������ʵ�������ȷ����?
[? ]
A����ϡ��ˮ����μ���ϡ��������Һ����������Һ Ag++2NH3��H2O=[Ag?(NH3)2]++2H2O
B����˫��ˮ��ϡ������Ե��ӡˢ��·�壺Cu+H2O2+2H+=Cu2++2H2O
C���ؾ�������ˮ��S2-?+?2H2O 2OH-?+?H2S
2OH-?+?H2S
D������ʯ��ˮ������մ���Һ��ϣ�Ca2++2OH��+2HCO3��=CaCO3��?+CO32��+2H2O?
�ο��𰸣�B
���������
�����Ѷȣ�һ��