1、选择题 常温下将两个铂电极插入200mLCuSO4溶液中进行电解,通电一定时间后,某一电极增重0.064g (设电解时该电极无氢气析出,且不考虑水解和溶液体积变化)。此时溶液中的pH为?
A.2
B.3-lg2
C.3
D.3+lg2
参考答案:A
本题解析:增重0.064g,即得到0.001mol的铜,转移0.002mol电子,此时会有0.002mol氢氧根离子放电,溶液中会得到0.002mol氢离子,此时,氢离子的浓度为0.01mol/L,PH为2.
本题难度:简单
2、选择题 用石墨作电极,电解质溶液中各离子浓度之比如下:c(Cu2+):c(Na+):c(Cl―)=1:2:4。在任何情况下,阴阳两极不可能同时发生的反应是(?)
A.阴极:2H++ 2e―=H2↑阳极:4OH――4e―=O2↑+2H2O
B.阴极:Cu2++2e―=Cu阳极:4OH――4e―=O2↑+2H2O
C.阴极:2H++2e―=H2↑阳极:2C1――2e―=Cl2↑
D.阴极:Cu2++2e―=Cu阳极:2C1――2e―=Cl2↑
参考答案:B
本题解析:该电解质溶液中的溶质为Cu Cl2和NaCl,且两都的物质的量之比为1:2;当电解该溶液时,第一阶段为电解Cu Cl2溶液;第二阶段为电解NaCl溶液,生成NaOH溶液;第三阶段为电解NaOH溶液;
A可能同时发生,在第三阶段电解NaOH溶液实质为电解水;
B不可能同时发生
C可能同时发生,在第三阶段电解NaCl溶液;
D可能同时发生,在第一阶段电解Cu Cl2溶液
本题难度:一般
3、填空题 (16分)草酸(H2C2O4)是一种二元弱酸,主要用作还原剂和漂白剂。草酸的盐可用作碱土金属离子的广谱沉淀剂。
(1)40 ℃时混合一定体积的0.1mol/L H2C2O4溶液与一定体积0.01mol/L酸性KMnO4溶液,填写表中空格。
温度
| v(H2C2O4)
| v(KMnO4)
| KMnO4褪色时间
|
40 ℃
| 10 ml
| 10 ml
| 40 s
|
40 ℃
| 20 ml
| 20 ml
| ?
|
(2)用甲基橙作指示剂,通过酸碱滴定可测定草酸溶液浓度。甲基橙是一种常用的酸碱指示剂,甲基橙(用化学式HIn表示)本身就是一种有机弱酸,其电离方程式为:HIn H++In―。则酸根离子In―的颜色是?。甲基橙的酸性与草酸相比,?(填前者强、前者弱、十分接近、无法判断)。
H++In―。则酸根离子In―的颜色是?。甲基橙的酸性与草酸相比,?(填前者强、前者弱、十分接近、无法判断)。
(3)常温下有pH均为3的盐酸和草酸溶液各10 ml,加水稀释,在答题卷上画出稀释过程中两种溶液中c(H+)变化的示意图并作必要的标注。
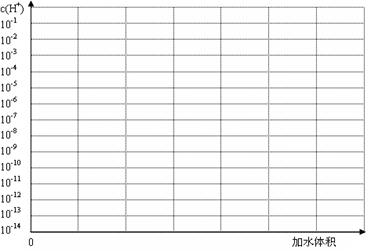
(4)常温下MgC2O4的Ksp=8.1×10-5,已知当溶液中某离子的浓度≤10-5 mol/L时可认为该离子已沉淀完全。现为了沉淀1 L0.01 mol/LMgCl2溶液中的Mg2+,加入100 mL0.1 mol/L的(NH4)2C2O4溶液,通过计算判断Mg2+是否已沉淀完全。
(5)(NH4)2C2O4溶液因NH4+水解程度稍大于C2O42-而略显酸性,0.1 mol/L(NH4)2C2O4溶液pH值6.4。现有某未知溶液,常温下由水电离出的c(H+)=1.0×10-5mol/L,该溶液pH可能是?(填字母)。
A.5? B.6 ? C.7?D.9
参考答案:(1)40 s (2分)
(2)黄色?前者弱(各2分)
(3)如图(3分,起点、终点各1分,斜率1分)
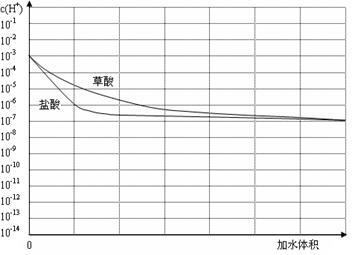
(4)MgCl2与(NH4)2C2O4恰好完全反应,但有
MgC2O4(s)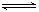 Mg2+(aq)+C2O42-(aq),c(Mg2+)・c(C2O42-)=Ksp=8.1×10-5,
Mg2+(aq)+C2O42-(aq),c(Mg2+)・c(C2O42-)=Ksp=8.1×10-5,
而c(Mg2+)=c(C2O42-),
c(Mg2+)=(8.1×10-5)-1/2=9×10-3 mol/L>10-5 mol/L
故Mg2+未沉淀完全。(4分)
(5)ABCD (3分,选对1个得1分,选对2个得2分,选对3个以上得3分)
本题解析:(1)反应速率与反应物的浓度有关,与反应物的物质的量多少无关,草酸和高锰酸钾的浓度并没有发生变化,而且温度也没有改变,所以反应速率是不变的,即褪色时间是不变的。
(2)甲基橙的变色范围是3.1~4.4,小于3.1时显红色,大于4.4时显黄色。根据甲基橙的电离方程式可知,当溶液碱性增强时平衡是向正反应方向移动的,所以该酸根的颜色是显黄色的。因为草酸钠溶液水解显碱性,此时甲基橙显黄色。若草酸的酸性弱于甲基橙的,则在草酸溶液中甲基橙显黄色,所以通过颜色的变化无法判断滴定终点。因此草酸的酸性要强于甲基橙的,这样在滴定过程中颜色才能发生变化。
(3)盐酸是强酸,草酸是弱酸,存在电离平衡,所以在稀释过程中盐酸中氢离子的浓度始终小于草酸中氢离子的浓度。但当无限稀释时二者的PH均要无限接近7。
(4)1 L0.01 mol/LMgCl2溶液中的Mg2+的物质的量是0.01mol,100 mL0.1 mol/L的(NH4)2C2O4溶液的物质的量也是0.01mol,即二者恰好反应。根据溶解平衡MgC2O4(s)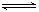 Mg2+(aq)+C2O42-(aq)可知c(Mg2+)・c(C2O42-)=Ksp=8.1×10-5
Mg2+(aq)+C2O42-(aq)可知c(Mg2+)・c(C2O42-)=Ksp=8.1×10-5
因为c(Mg2+)=c(C2O42-),所以c(Mg2+)=(8.1×10-5)-1/2=9×10-3 mol/L>10-5 mol/L
故Mg2+未沉淀完全。
(5)常温下由水电离出的c(H+)=1.0×10-5mol/L,说明该溶液中水的电离是被促进的,若只有阳离子水解,则溶液显酸性,即此时溶液的pH为5。若只有阴离子水解,则溶液显碱性,此时溶液中的c(OH-)=1.0×10-5mol/L,则溶液中的c(H+)=1.0×10-9mol/L所以溶液的pH是9。若溶液阴离子和阳离子同时都水解。若阳离子的水解程度大于阴离子的水解程度,则溶液显碱性;若阳离子的水解程度小于阴离子的水解程度,则溶液显酸性;阳离子的水解程度和阴离子的水解程度相同,则溶液显中心,所以选项A、B、C、D均正确。
本题难度:一般
4、选择题 已知HF比CH3COOH易电离。关于物质的量浓度、体积都相同的NaF溶液和CH3COONa溶液,下列说法正确的是(? )
A.两溶液相比较,NaF溶液中的离子总数较多
B.在相同条件下,两溶液的pH大小为: CH3COONa< NaF
C.NaF溶液中:c(H+)+c(HF)= c(OH-)+ c(F-)
D.CH3COONa溶液中:c(CH3COO-)>c(Na+)>c(OH-)>c(H+)
参考答案:A
本题解析:A:在NaF溶液中:c(H+)+c(Na+)= c(OH-)+ c(F-)
在CH3COONa溶液中:c(H+)+c(Na+)= c(OH-)+ c(CH3COO-)
由于HF比CH3COOH易电离,则物质的量浓度、体积都相同的NaF溶液和CH3COONa溶液相比,前者的碱性弱,c(OH-)相对较小,而c(H+)相对较大,故由以上两式可知,NaF溶液中的离子总数较多,正确
B:由“越弱越水解”可知NaF溶液水解程度相对较小,pH较小,不正确
C:违反了电荷守恒,正确的为c(H+)+c(Na+)= c(OH-)+ c(F-),排除
D:由于CH3COO-部分水解,溶液呈碱性,故c(Na+)>c(CH3COO-)>c(OH-)>c(H+),排除
答案为A
本题难度:一般
5、选择题 pC类似pH,是指极稀溶液中溶质物质的量浓度的常用对数负值。如某溶液溶质的浓度为1×10-3mol/L,则该溶液中溶质的pC=3。下列叙述正确的是
A.某温度下任何电解质的水溶液中,pC(H+) +pC(OH-)=14
B.0.01 mol/L的CaCl2溶液中逐滴加入纯碱溶液,滴加过程中pC(Ca2+)逐渐减小
C.用0.01 mol/L的盐酸滴定某浓度的NaOH溶液,滴定过程中pC(H+)逐渐增大
D.某温度下,难溶性离子化合物AB的Ksp=1.0×10-10, 其饱和溶液中pC(A+)+pC(B-)=10
参考答案:D
本题解析:A项中只有常温下才有pC(H+) +pC(OH-)=14,错误;B项在0.01 mol/L的CaCl2溶液中逐滴加入纯碱溶液,在滴加过程中C(Ca2+)逐渐减小,则pC(Ca2+)逐渐增大,错误;C项用0.01 mol/L的盐酸滴定某浓度的NaOH溶液,在滴定过程中C(H+)逐渐增大,则pC(H+)逐渐减小,错误;D项根据饱和溶液中c(A+)×c(B-)=Ksp=1.0×10-10,则pC(A+)+pC(B-)=10,正确。
本题难度:一般