1��ѡ���� �������ӷ���ʽ��ȷ���ǣ�������
A��̼�����ϡHNO3��CO32-+2H+=CO2��+H2O
B��Cu��AgNO3��Һ��Cu+2Ag+=Cu2++2Ag
C��Fe��ϡH2SO4��2Fe+6H+=2Fe3++3H2��
D��Ba��OH��2��ϡH2SO4��Ba2++SO42-=BaSO4��
�ο��𰸣�q��̼�����ϡHNO3��Ӧ�����ӷ���ʽΪ��CqCO3+2H+=CO2��+H2O+Cq2+����q����
B��Cu��q��NO3��Һ��Ӧ������������ͭ����Ӧ�����ӷ���ʽΪ��Cu+2q��+=Cu2++2q�ߣ���B��ȷ��
C��Fe��ϡH2SO4����Ӧ����������������������Ӧ���ӷ���ʽΪ��Fe+2H+=Fe2++H2������C����
D��Bq��OH��2��ϡH2SO4��Ӧ�������ᱵ������ˮ����Ӧ���ӷ���ʽΪ��2OH-+2H++Bq2++SO42-=BqSO4��+H2O����D����
��ѡB��
���������
�����Ѷȣ���
2������� �������������������й㷺Ӧ�á�
��ҵ�����ؾ�ʯ����Ҫ�ɷ�BaSO4��Ϊԭ���Ʊ�BaCl2���乤������ʾ��ͼ���£�
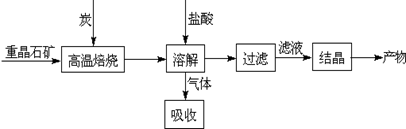
ij�о�С��������ϵã�
BaSO4��s��+4C��s�� 4CO��g��+BaS��s����H1=+571.2kJ?mol-1?��
4CO��g��+BaS��s����H1=+571.2kJ?mol-1?��
BaSO4��s��+2C��s�� 2CO2��g��+BaS��s����H2=+226.2kJ?mol-1? ��
2CO2��g��+BaS��s����H2=+226.2kJ?mol-1? ��
��1���ù���NaOH��Һ�������壬�õ����ơ��÷�Ӧ�����ӷ���ʽ��?��
��2����ӦC��s��+CO2��g�� 2CO��g���ġ�H= ?��
2CO��g���ġ�H= ?��
��3��ʵ�������б�����������̿��ͬʱ��Ҫͨ���������Ŀ��������
�ٴ�ԭ�ϽǶȿ���?��
�ڴ������Ƕȿ����٢�Ϊ���ȷ�Ӧ��̿��������Ӧ����ά�ַ�Ӧ������¡�
��4����С��ͬѧ���BaSO4��ˮ�еij����ܽ�ƽ������һ���о��������Ϸ�����ij�¶�ʱBaSO4��ˮ�еij����ܽ�ƽ��������ͼ��ʾ��

��С��ͬѧ����������ֹ۵㣺
�ٵ�����SO42-����Һ�м���Ba2+ ʹSO42-������ȫ�����ʱSO42-����Һ�е�Ũ��Ϊ0
�ڼ���Na2SO4����ʹ��Һ��a��䵽b��
��ͨ����������ʹ��Һ��d��䵽c��
��d����BaSO4��������
������ȷ����?������ţ���
��ijȼ�ϵ����CaHSO4����Ϊ����ʴ���H+��������ṹ��ͼ��ʾ������ܷ�Ӧ�ɱ�ʾΪ2H2+O2�T2H2O��

��ش�
��5��H+��?��ͨ�����������ʴ��ݵ���һ������a����b����
��6��b���Ϸ����ĵ缫��Ӧ�� ?��
�ο��𰸣�27����12�֣�ÿ��2�֣�
��1��H2S+2OH- =2S2-+H2O
��2��+172.5 kJ?mol-1
��3��ʹBaSO4�õ���ֵĻ�ԭ�����BaS�IJ���
��4����
��5��a
��6��O2+4e-+4H+�T2H2O
���������
��1�����յ�������H2S���õ����ơ��÷�Ӧ�����ӷ���ʽH2S+2OH- =2S2-+H2O ��
��2�����ݸ�˹���ɣ��٣���*2��/2��+172.5 kJ?mol-1
��3��ʹBaSO4�õ���ֵĻ�ԭ�����BaS�IJ���
��4�����������SO42-����Һ�е�Ũ�ȶ�����Ϊ0������
�ڼ���Na2SO4����ʹ��Һ��a��䵽b�㣬�൱��������SO42-��Ũ�ȣ���ʱ��Һ�б�����Ũ�ȼ�С�ģ�����
��?ͨ����������ʹ��Һ��d��䵽c�㣬������SO42-��Ũ�Ȼ��DZ�����Ũ�ȶ������ӵģ�����
��d����������SO42-��Ũ�Ȼ��DZ�����Ũ�ȶ��DZȽ�С�ģ���ʱ�ܶȻ������ӻ�����С��δ�ܳ�����������ȷ���Ǣܡ�
��5��b�缫����������������ԭ������������ƶ���ѡa
��6��b�缫��������������ԭ��Ӧ�����������Ե�����У��ʷ���ʽΪO2+4e-+4H+�T2H2O
�����Ѷȣ�����
3��ѡ���� �������ӷ���ʽ��ȷ����
[? ]
A��H2SO4��Ba(OH)2��Һ��Ӧ Ba2++OH-+H++SO42-===BaSO4��+H2O
B��CuSO4��Һ����H2S���壺Cu2++H2S===CuS��+2H+
C��AlCl3��Һ�м��������Ũ��ˮ�� Al3++4NH3��H2O===[Al(OH)4]-+4NH4++2H2O
D�����������Ũ�ȵ�Ba(OH)2ϡ��Һ��NH4HCO3ϡ��Һ��ϣ�
Ba2++2OH-+NH4++HCO3-===BaCO3��+NH3��H2O+H2O
�ο��𰸣�BD
���������
�����Ѷȣ�һ��
4��ѡ���� �������ӷ���ʽ��ȷ���ǣ�������
A�������������Һ�м���Ba��OH��2��ҺʹSO42-ǡ����ȫ������2H++SO42-+Ba2++2OH-=BaSO4��+2H2O
B����NaHS��Һ�еμ�����CuCl2��Һ��S2-+Cu2+=CuS��
C����������Һ�еμӹ��������[Ag��NH3��2]++OH-+3H++Br-=AgBr��+2NH4++H2O
D��ˮ���ᣨ

����������Na2CO3��Һ��ϣ�

�ο��𰸣�A�������������Һ�м���Ba��OH��2��ҺʹSO42-ǡ����ȫ������������غ�������������1��1��H++SO42-+Ba2++OH-=BaSO4��+H2O����A����
B����NaHS��Һ�еμ�����CuCl2��Һ������ͭ������HS-+Cu2+=CuS��+H+����B����
C����������Һ�еμӹ��������ᣬ�������廯�����ܳ��������ӷ���ʽΪ��[Ag��NH3��2]++OH-+3H++Br-=AgBr��+2NH4++H2O����C��ȷ��
D��ˮ����������̼���Ʒ�Ӧ�Ȼ���Ӧ����������̼�����ǻ���Ӧֻ������̼�����ƣ����ӷ���ʽ�е����Ͳ������D����
��ѡC��
���������
�����Ѷȣ�һ��
5������� ����Լռ����������71%������ʮ�־�Ŀ���DZ����ijУ�о���ѧϰС��ͬѧ�Ծ���������������Ũ����ˮ����Ҫ��NaCl��MgSO4�������о���
��1��ʵ��ʱ����������ƽ����500mL0.20mol/LNaOH��Һ�������������NaOH��������
��2��ȡ��������������Ũ����ˮ100mL������200mL0.20mol/LNaOH��Һ��ǡ�ð����е�Mg2+��ȫ��������Ũ����ˮ��Mg2+�����ʵ���Ũ��Ϊ���٣�
��3���о�С��ͬѧ������������ȫת��Ϊ��ˮMgCl2����������״̬�½��е�⣬�ɵñ�״����Cl2��������
�ο��𰸣���1���������Ƶ����ʵ���n��NaOH��=C��NaOH����V=0.20mol/L��0.5L=0.10mol��
����NaOH������m��NaOH��=n��NaOH��?M��NaOH���T0.10mol��40g/mol=4.0g��
�𣺹���NaOH������Ϊ4.0g��?
��2����������þ�����ʵ���Ϊx��
? MgCl2 +2NaOH�TMg��OH��2��+2NaCl
? 1? 2
?x? ?0.20L��0.20mol/L
? ?1x=20.20L��0.20mol/L
? x=0.02mol
?����c��Mg2+��=0.02mol?0.1L=0.2mol/L?
��Ũ����ˮ��Mg2+�����ʵ���Ũ��Ϊ0.2mol/L��
��3�������������ʵ���Ϊy��
? MgCl2�����ڣ�??ͨ��?.? Mg+Cl2��
? ?1? 1
? 0.02mol? y
? 1?0.02mol=1y
? y=0.02mol
? V��Cl2��=0.02mol/L��0.1L��22.4L/mol=0.448L?
�𣺿ɵñ�״��������0.448L��
���������
�����Ѷȣ�һ��