1、选择题 下列实验操作正确的是
A.用托盘天平称取5.5gKCl固体
B.在酸碱中和滴定实验中,锥形瓶用蒸馏水洗涤后再用待测液润洗
C.将干燥的pH试纸浸入某溶液一会儿后取出,与标准比色卡比较以测定该溶液的pH
D.配制0.1mol?L-1的硫酸溶液时,将量取的浓硫酸放入容量瓶中加水稀释
参考答案:A
本题解析:分析:A.托盘天平读数时只能读到小数点后一位;
B.在酸碱中和滴定实验中,锥形瓶用蒸馏水洗涤后再用待测液润洗,导致待测液的浓度测量结果偏大;
C.PH试纸不能直接插入到待测液中;
D.容量瓶上有刻度,热胀冷缩影响其配制溶液的精确度,不能在容量瓶中稀释浓硫酸,应在烧杯中稀释后转移到容量瓶中;
解答:A.托盘天平只能称准到0.1g,所以能用托盘天平称取5.5gKCl固体,故A正确;
B.在酸碱中和滴定实验中,锥形瓶用蒸馏水洗涤后再用待测液润洗,待测液的实际取量大于计算取量,而实际计算时仍用量取的体积数,V待测值小于V真实值,导致待测液的浓度测量结果偏大,故B错误;
C.将干燥的pH试纸浸入某一溶液一会儿后取出,会玷污溶液,正确使用方法是用玻璃棒点蘸取溶液点滴到试纸的中部与标准比色卡比较,故C错误;
D.容量瓶上有刻度线,稀释浓硫酸放热,影响其精确度,甚至放出的热会把容量瓶炸裂,所以应在烧杯中稀释后转移到容量瓶中,故D错误;
故选A.
点评:本题考查了实验基本操作,掌握托盘天平、滴定中的锥形瓶、PH试纸、容量瓶的正确使用方法是解答本题的关键,题目难度不大.
本题难度:困难
2、选择题 下列仪器常用于物质分离的是
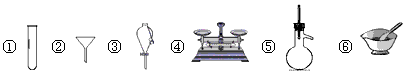
[? ]
A.①③⑤
B.②③⑤
C.②④⑤
D.①②⑥
参考答案:B
本题解析:
本题难度:简单
3、选择题 在容量瓶上无需有的标记是( )
A.浓度
B.温度
C.标线
D.容量
参考答案:因容量瓶上标有:温度、规格、刻度线,故选:A.
本题解析:
本题难度:一般
4、填空题 Ⅰ.如图所示是几种实验中常用的仪器:
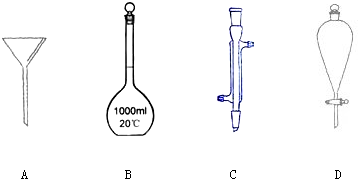
写出序号所代表的仪器的名称:A______;B______;C______;D______.
Ⅱ.实验室要配制100mL2mol/LNaOH溶液,请回答下列问题:
(1)配制过程中使用的化学仪器有______(填选项的字母).
A.烧杯 B.100mL容量瓶 C.漏斗 D.胶头滴管 E.玻璃棒
(2)用托盘天平称取氢氧化钠,其质量为______g.
(3)下列主要操作步骤的正确顺序是______(填序号).
①称取一定质量的氢氧化钠,放入烧杯中,用适量蒸馏水溶解;
②加水至液面离容量瓶颈刻度线下1-2厘米时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切;
③待冷却至室温后,将溶液转移到100mL容量瓶中;
④盖好瓶塞,反复上下颠倒,摇匀;
⑤用少量的蒸馏水洗涤烧杯内壁和玻璃棒2~3次,洗涤液转移到容量瓶中.
(4)如果实验过程中缺少步骤⑤,会使配制出的NaOH溶液浓度______(填“偏高”或“偏低”或“不变”).
参考答案:Ⅰ图中A漏斗;B容量瓶;C冷凝管;D分液漏斗,故答案为:漏斗;容量瓶;冷凝管;分液漏斗;
Ⅱ(1)选取容量瓶的规格应该等于或稍微大于需要配制溶液的体积,所以应该选取100mL的容量瓶,故答案为:C;(2)m=CVM=2mol/L×0.1L×40g/mol=8.0g,故答案为:8.0;
(3)实验操作的步骤:计算、称量、溶解、移液、洗涤移液、定容、摇匀等操作进行排序,所以其排列顺序为:①③⑤②④,故答案为:①③⑤②④;
(4)没有洗涤烧杯内壁和玻璃棒会使溶质的物质的量偏小,配制溶液浓度偏低,故答案为:偏低.
本题解析:
本题难度:一般
5、简答题 先选择填空,再简要说明作此选择的理由.
(1)某试管内装有约占容积
的溶液,则溶液的体积是______,因为______.
A、约1mL?B、约3mL?C、约25mL?D、无法判断
(2)拟在烧杯中于加热条件下配制某溶液50mL,应选择的烧杯是______,因为______.
A、400mL烧杯?B、250mL烧杯?C、100mL烧杯?D、50mL烧杯.
参考答案:(1)试管有多种规格,试管的容积有大有小,题目没有明确试管的规格和体积,则占其容积的1/10的溶液体积是无法确定的,
故答案为:D;试管有多种规格,试管的容积有大有小,题目没有明确试管的规格和体积,则占其容积的1/10的溶液体积是无法确定的;
(2)因在配制溶液的过程中用烧杯来溶解溶质,一般情况下选用烧杯的容积应比所配溶液的体积大一倍,
故答案为:C;配制溶液的过程中用烧杯来溶解溶质,一般情况下选用烧杯的容积应比所配溶液的体积大一倍为宜.
本题解析:
本题难度:一般