1、填空题 Ⅰ选择下列实验方法分离物质,将分离方法的序号填在横线上.
A.萃取?B.分液?C.过滤?D.加热分解?E.蒸发?F.蒸馏
(1)分离饱和食盐水与沙子的混合物______;
(2)从碘的水溶液里提取碘______;
(3)分离水和汽油的混合物______;
(4)分离CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)的混合物______.
Ⅱ将以下几种物质中,按要求将正确答案填写在相应的空格内
①干燥的食盐晶体;?②液态氯化氢;?③水银;?④蔗糖;
⑤CO2;?⑥KNO3溶液;?⑦氯气
以上物质中能导电的是______;属于电解质的是______;属于非电解质的是______;(填正确答案的序号)
参考答案:Ⅰ(1)沙子不溶于水,则不溶性固体与溶液的分离方法为过滤,故答案为:C;
(2)碘在水中的溶解度小,在有机溶剂中的溶解度大,利用萃取来分离,故答案为:A;
(3)水与汽油不相溶,分层,利用分液来分离,故答案为:B;
(4)四氯化碳、甲苯互溶,但沸点不同,利用蒸馏来分离,故答案为:F;
Ⅱ含自由移动的离子或自由移动的电子,则能导电,给出的物质只有③⑥能导电;在水溶液中或熔化状态下能导电的化合物为电解质,则①②为电解质;在水溶液中和熔化状态下均不能导电的化合物为非电解质,则④⑤为非电解质,故答案为:③⑥;①②;④⑤.
本题解析:
本题难度:简单
2、简答题 请按要求填空:
I.现有:①612C与614C、②O2与O3、③正丁烷与异丁烷、④金刚石与石墨、⑤冰与水、⑥乙醇与二甲醚.请用序号填写对应的分类:
(1)互为同位素的是______;
(2)互为同素异形体的是______;
(3)互为同分异构体的是______;
(4)属于同一化合物的是______.
Ⅱ.现有以下物质:①NaCl晶体②液态(纯)H2SO4③液态的(纯)醋酸④汞(金属)⑤纯蔗糖(C12H22O11)⑥酒精(C2H5OH)⑦熔化的KNO3,请回答下列问题(用序号):
(1)以上物质中能导电的是______,
(2)以上物质中属于电解质的是______,
(3)以上物质中属于非电解质的是______,
(4)以上物质中溶于水后形成的水溶液能导电的是______.
参考答案:Ⅰ.(1)具有相同质子数,不同中子数(或不同质量数)同一元素的不同核素互为同位素,612C与614C是碳元素的不同核素属于同位素.故答案为:①;
(2)同素异形体是同种元素形成的不同单质,O2与O3是氧元素的不同单质,金刚石和石墨是碳元素的不同单质属于同素异形体.故答案为:②④;
(3)具有相同分子式而结构不同的化合物互为同分异构体,正丁烷和异丁烷分子式都是C4H10,结构不同属于同分异构体,乙醇与二甲醚分子式相同,结构不同,互为同分异构体,故答案为:③⑥;
(4)冰是固态的水,冰和水均由水分子构成,属于同种物质,故答案为:⑤;
Ⅱ.(1)④汞中有自由电子,所以能导电;⑦熔化的KNO3中有自由移动的离子,所以能导电;①NaCl晶体、②液态(纯)H2SO4、③液态的(纯)醋酸、⑤纯蔗糖(C12H22O11)、⑥酒精(C2H5OH)没有自由移动的离子或自由电子,所以不能导电,
故答案为:④⑦;
(2)在水溶液里或熔融状态下能导电的化合物是电解质,所以①NaCl晶体、②液态(纯)H2SO4③液态的(纯)醋酸、⑦熔化的KNO3是电解质;
故答案为:①②③⑦;
(3)非电解质是在水溶液里或熔融状态下都不能导电的化合物,所以⑤纯蔗糖(C12H22O11)、⑥酒精(C2H5OH)是非电解质;
故答案为:⑤⑥;
(4)水溶液能导电的原因是溶液中含有自由移动的离子;①NaCl晶体、②液态(纯)H2SO4、③液态的(纯)醋酸、⑦熔化的KNO3溶于水后形成的水溶液能导电;
故答案为:①②③⑦.
本题解析:
本题难度:简单
3、选择题 有关电解质的说法正确的是( )
A.碳酸钙难溶于水,但碳酸钙是电解质
B.SO3水溶液的导电性很好,所以SO3是电解质
C.液态的铜导电性很好,所以铜是电解质
D.Na2O液态时能导电,所以Na2O是电解质
参考答案:AD
本题解析:
本题难度:一般
4、简答题 下图为五个椭圆交叉构成的图案,椭圆内分别写了C2H5OH、CO2、Fe2O3、FeCl3和NaOH五种物质,图中相连的两种物质均可归为一类,相交的部分A、B、C、D为其相应的分类标准代号.请回答下列问题:
(1)两种物质都是非电解质的是______(填分类标准代号,下同),两种物质在水溶液中都能导电的是______.
(2)分类标准代号C表示______(多项选择)
a.两物质都是电解质b.两物质都可与酸反应
c.两物质都有氧化性d.两物质可以通过一步反应相互转化
(3)上述五种物质中的某一物质能与某种强酸反应生成上述中的另一种物质,该反应的化学方程式为______.
(4)图中相连的两种物质可归为一类,又能相互反应的是______(填分类标准代号),其反应的基本类型是______反应.
(5)用洁净的烧杯取25mL蒸馏水,加热至沸腾,向烧杯中逐滴加入上述五种物质中的某一物质的饱和溶液,加热呈红褐色,得到的分散系称为______,该反应的化学方程式为______.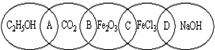
参考答案:(1)在水溶液里或熔融状态下都不导电的化合物是非电解质,乙醇和二氧化碳都是非电解质,故选A;
含有自由移动的离子的水溶液就能导电,易溶性的电解质溶液就能导电,故选D.
故答案为:A;D;
?(2)a、Fe2O3在熔融状态下能导电,FeCl3的水溶液能导电,所以这两种物质都是电解质,故a正确.
b、Fe2O3能和酸反应生成盐和水,FeCl3和一般的酸不反应,故b错误.
c、Fe2O3和FeCl3中的铁元素都是最高价,所以都有氧化性,故c正确.
d、Fe2O3和盐酸反应生成氯化铁是一步转化;加热氯化铁溶液至蒸干,发生的反应有:氯化铁水解生成氢氧化铁,氢氧化铁加热分解生成氧化铁,所以是两步反应,故d错误.
故选ac;
?(3)某一物质能与某种强酸反应生成上述中的另一种物质,所以这两种物质应有相同的元素,且化合价不变,所以是氧化铁和氯化铁,
化学反应方程式为:Fe2O3+6HCl=2FeCl3+3H2O,故答案为:Fe2O3+6HCl=2FeCl3+3H2O;
(4)根据各物质的性质分析,只有氯化铁和氢氧化钠反应生成氢氧化铁沉淀和氯化钠,该反应中没有化合价的变化,所以是复分解反应.
故答案为:D;?复分解反应;
(5)该方法是制作氢氧化铁胶体,反应方程式为FeCl3+3H2O?△?.?Fe(OH)3(胶体)+3HCl
故答案为:胶体;FeCl3+3H2O?△?.?Fe(OH)3(胶体)+3HCl.
本题解析:
本题难度:一般
5、选择题 下列物质中属于非电解质的是( )
A.氯化钾的水溶液
B.液态氯化氢
C.气态甲烷
D.作电极的碳棒
参考答案:A.氯化钾的水溶液,是混合物,既不是电解质,也不是非电解质,故A错误;
B.液态氯化氢,是纯净物,氯化氢水溶液能导电,是由于电离出自由移动的氢离子和氯离子,氯化氢是化合物,属于电解质,故B错误;
C.气态甲烷,甲烷难溶于水,水溶液中和熔融状态下都不能够导电,是非电解质,故C正确;
D.作电极的碳棒是单质,不是化合物,所以不是电解质,也不是非电解质,故D错误;
故选C.
本题解析:
本题难度:一般