1、选择题 NA表示阿伏伽德罗常数的值,下列说法正确的是( )
A.5.6g铁粉在0.1mol氯气中充分燃烧,转移电子数为0.3NA
B.1mol Na2O2与足量H2O充分反应,转移的电子数为2NA
C.7.8g Na2O2中含有的阴离子数等于0.1NA
D.0.5mol雄黄(As4S4,结构如图)含有NA个S-S键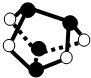
参考答案:A、5.6g铁粉在0.1mol氯气中充分燃烧生成氯化铁,5.6g铁粉反应需要0.15mol氯气,所以氯气不足,根据氯气计算转移的电子数,所以反应转移电子数为0.1mol×2×NAmol-1=0.2NA,故A错误;
B、过氧化钠中被氧化的O原子与被还原的O氧原子物质的量之比为1:1,所以1mol Na2O2与足量H2O充分反应,转移的电子数为1mol×1×NAmol-1=NA,故B错误;
C、过氧化钠有钠离子和过氧根离子构成,7.8g Na2O2中含有的阴离子数为7.8g78g/mol×NAmol-1=NA,故C正确;
D、As原子原子半径比S原子大,由结构可知,黑色球为As原子,白色球为S原子,As4S4分子中不含S-S键,故D错误.
故选:C.
本题解析:
本题难度:一般
2、选择题 设NA表示阿伏加德罗常数,下列说法不正确的是( )
A.甲烷的摩尔质量与NA个甲烷分子的质量在数值上相等
B.NA个氧分子和NA个氢气分子的质量比为16:1
C.28g氮气所含的原子数目为NA
D.NA个硫酸分子中所含的氧原子个数与4NA个水分子中所含氧原子个数相等
参考答案:A、甲烷的摩尔质量为16g/mol,NA个甲烷分子的物质的量为1mol,质量为1mol×16g/mol=16g,二者在数值上相等,故A正确.
B、NA个氧分子和NA个氢气分子的物质的量都为1mol,物质的量相同,质量之比等于摩尔质量之比为32g/mol:2g/mol=16:1,故B正确;
C、28g氮气的物质的量为28g28g/mol=1mol,每个氮气分子含有2个氮原子,含有氮原子数目为为1mol×2×NAmol-1=2NA,故C错误;
D、每个硫酸分子含有4个氧原子,NA个硫酸分子含有氧原子数为4NA,每个水分子含有1个氧原子,4NA个水分子含有的氧原子数目为4NA,故D正确.
故选:C.
本题解析:
本题难度:简单
3、选择题 以NA表示阿伏加德罗常数,下列说法正确的是
[? ]
A.0.1mol Fe与足量盐酸反应,转移的电子数为0.3NA
B.28gCO中所含的原子数为2NA
C.0.1 mol Na2CO3溶液中,含有CO32-数为0.1NA
D.标准状况下,22.4 L苯的分子数为NA
参考答案:B
本题解析:
本题难度:简单
4、选择题 同温同压下,10mL A2气体与20mL B2气体恰好完全反应,生成20 mL C气体,则C的化学式应为
A.AB2
B.A2B
C.A2B4
D.AB