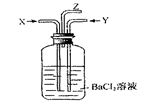
1��ѡ���� ̼��Ũ���Ṳ�Ȳ���������X��ͭ��Ũ���ᷴӦ����������Yͬʱͨ��ʢ�������Ȼ�����Һ��ϴ��ƿ�У���ͼ��������˵����ȷ���ǣ�?��
A��ϴ��ƿ�в����ij�����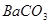
B����Z���ܳ�������������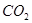
C��ϴ��ƿ�в����ij�����
D����Z���ܿ��к���ɫ�������
�ο��𰸣�D
�����������������֪��̼��Ũ���Ṳ�Ȳ�����X����ΪCO2��SO2�Ļ�����壬ͭ��Ũ���ᷴӦ������Y������NO2��ͬʱͨ��ʢ�������Ȼ�����Һ��ϴ��ƿ�У�NO2��SO2��ˮ��Ӧ���������NO��NO�ڿ������ֻ�����NO2��A��CO2�����Ȼ�����Ӧ���ӵ������ݳ���ϴ��ƿ�в������̼�ᱵ���������� B��CO2�����Ȼ�����Ӧ���ӵ���Z���ݳ�������C��SO2+H2O+NO2=H2SO4+NO��H2SO4�����Ȼ�����Ӧ����BaSO4������û��BaSO3���ɣ�����D����Ӧ���ɵ�NO��Z���ܿ�������е�������Ӧ����NO2���ʺ���ɫ����ȷ��
�����Ѷȣ�һ��
2��ʵ���� ��10�֣���ѧС��ͬѧ���ݻ�ѧ��ӦZn��2H2SO4(Ũ) ZnSO4��SO2����2H2O��ȡ22.4 L(��״��)SO2���塣ȡ65.0 gп����98%��ŨH2SO4(�ѣ�1.84 g��cm-3)110 mL��ַ�Ӧ��пȫ���ܽ⡣�����Ƶõ����壬��ͬѧ��Ϊ���ܻ���������Ϊ�ˣ���ѧС���ͬѧ���������ʵ��װ�ã�������ȡ���������̽����
ZnSO4��SO2����2H2O��ȡ22.4 L(��״��)SO2���塣ȡ65.0 gп����98%��ŨH2SO4(�ѣ�1.84 g��cm-3)110 mL��ַ�Ӧ��пȫ���ܽ⡣�����Ƶõ����壬��ͬѧ��Ϊ���ܻ���������Ϊ�ˣ���ѧС���ͬѧ���������ʵ��װ�ã�������ȡ���������̽����

��ش��������⣺
��1��װ��A������Һ�����������Ϊ?��98%��ŨH2SO4(�ѣ�1.84 g/cm3)�����ʵ���Ũ����?��
��2����д�����������ķ�Ӧ�����ӷ���ʽ?��
��3����װ��B��Ϊ������SO2������ѡ�������Լ��е�?������ţ���
A��NaOH��Һ? B��ŨH2SO4? C��KMnO4��Һ?
�ڿ�֤ʵһ������п����һ������Ũ���ᷴӦ�����ɵ������л���������ʵ��������?��
�ο��𰸣���1����Һ©��? 18.4 mol/L?��2��Zn��2H+===Zn2+��H2��?
��3���� B�� ��װ��E�к�ɫ��ĩ���ɫ��F����ˮ����ͭ����ɫ?��ÿ��2�֣�
����������Ÿ����������Ƿ�Һ©����C��H2SO4��=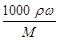 ��
��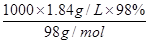 ��18.4?mol/L��?
��18.4?mol/L��?
��п��ϡ���ᷴӦ��������п�������������ӷ���ʽΪZn+2H+�TZn2++H2����
�Ǣٶ���������������������ܱ���Һ���գ����л�ԭ�ԣ��ܱ�ǿ��������Һ���գ�����������Һ�ʼ��ԣ����������Һ����ǿ�����ԣ�������������������Һ���������Һ���ն�������ѡB����?
���������л�ԭ�ԣ��ܽ���ɫ��CuO��ԭΪ��ɫ��Cu��������ˮ��ˮ��ʹ��ˮ����ͭ����ɫ������������������������ǣ�װ��E�к�ɫ��ĩ���ɫ��F����ˮ����ͭ����ɫ��
�����Ѷȣ�һ��
3��ʵ���� ��18�֣�
����ͬѧ�����ἰ���ε�ijЩ�����н���������ʵ��̽����
[ʵ��һ ]̽��Ũ�����������
]̽��Ũ�����������
 ������ʵ���ҳ��õ�ҩƷ��������ͼ��ʾ��ʵ��װ�ú���װ�üס����гֺͼ���װ��ʡ�ԣ�
������ʵ���ҳ��õ�ҩƷ��������ͼ��ʾ��ʵ��װ�ú���װ�üס����гֺͼ���װ��ʡ�ԣ�
 ��1����װ������ϴ�������ȱ�ݣ���ȱ����?__________
��1����װ������ϴ�������ȱ�ݣ���ȱ����?__________ _______________________?___��
_______________________?___��
 ��2��װ�ü��з�Ӧ�Ļ�ѧ����ʽ��___________?___��
��2��װ�ü��з�Ӧ�Ļ�ѧ����ʽ��___________?___��
 ��3��װ�����е��Լ���_____________________________________________________��
��3��װ�����е��Լ���_____________________________________________________��
[ʵ��� ]̽��ij���������ι����Ƿ����
]̽��ij���������ι����Ƿ����
 ��4�������������ͬѧ�������ʵ�鷽����
��4�������������ͬѧ�������ʵ�鷽����
ʵ�����
| Ԥ������ͽ���
|
 ? ?
| ?
|
[ʵ����]��KHSO4��ȡH2O2��������������
 �������ϵ�֪����ҵ���õ��KHSO4������Һ��ȡH2O2��ʾ��ͼ���£�
�������ϵ�֪����ҵ���õ��KHSO4������Һ��ȡH2O2��ʾ��ͼ���£�
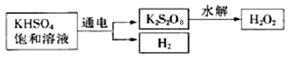

 �����ô˷���ȡһ��Ũ�ȵ�H2O2������������ʵ��ⶨH2O2�����������������ӷ���ʽ��2MnO4�D��5H2O2��6H����2Mn2����8H2O��5O2����
�����ô˷���ȡһ��Ũ�ȵ�H2O2������������ʵ��ⶨH2O2�����������������ӷ���ʽ��2MnO4�D��5H2O2��6H����2Mn2����8H2O��5O2����
 ��ȡ5.00 mL H2O2��Һ���ܶ�Ϊ1.00 g/mL��������ƿ�м�ˮϡ�ͣ��ټ�ϡ�����ữ��
��ȡ5.00 mL H2O2��Һ���ܶ�Ϊ1.00 g/mL��������ƿ�м�ˮϡ�ͣ��ټ�ϡ�����ữ��
 ����0.1000 mol/L KMnO4��Һ�ζ���
����0.1000 mol/L KMnO4��Һ�ζ���
 ����ͬ�������ζ�����������KMnO4��Һ������ֱ�Ϊ20.00 mL��19.98 mL��20.02 mL��
����ͬ�������ζ�����������KMnO4��Һ������ֱ�Ϊ20.00 mL��19.98 mL��20.02 mL��
 ��ش�
��ش�
 ��5����ⱥ��KHSO4��Һʱ�������ĵ缫��ӦʽΪ____________________________��
��5����ⱥ��KHSO4��Һʱ�������ĵ缫��ӦʽΪ____________________________��
 ��6���������У������һ��KMnO4��Һ����Һ�Ϻ�ɫ��ʧ���������ŵζ�������Mn2�������࣬��Һ�Ϻ�ɫ��ʧ���ʼӿ졣Mn2����������_____________?___��
��6���������У������һ��KMnO4��Һ����Һ�Ϻ�ɫ��ʧ���������ŵζ�������Mn2�������࣬��Һ�Ϻ�ɫ��ʧ���ʼӿ졣Mn2����������_____________?___��
 ��7��ԭH2O2��Һ�����ʵ�����������__________?_____?____��
��7��ԭH2O2��Һ�����ʵ�����������__________?_____?____��
�ο��𰸣���18��
 ��1��װ���Ҳ�Ӧ��ƿ��? (2��)
��1��װ���Ҳ�Ӧ��ƿ��? (2��)
 ��2��Cu��2H2SO4(Ũ)
��2��Cu��2H2SO4(Ũ) CuSO4��SO2����2H2O? (2��)
CuSO4��SO2����2H2O? (2��)
 ����C��2H2SO4(Ũ)
����C��2H2SO4(Ũ) CO2����2SO2����2H2O������������Ҳ���֣�
CO2����2SO2����2H2O������������Ҳ���֣�
 ��3������������Һ��������������Һ�ȣ�? (2��)
��3������������Һ��������������Һ�ȣ�? (2��)
 ��4����һ֧�Թ��м����������壬��ˮ�ܽ⣬�ٵμӼ���KSCN��Һ��? (2��)
��4����һ֧�Թ��м����������壬��ˮ�ܽ⣬�ٵμӼ���KSCN��Һ��? (2��)
����Һ��Ϊ��ɫ��˵���ù����ѱ��ʣ�����Һδ���ɫ��˵���ù���û�б���? (2��)
 ��5��2HSO4�D�D2e����S2O82����2H������2SO42�D��2e����S2O82����? (3��)
��5��2HSO4�D�D2e����S2O82����2H������2SO42�D��2e����S2O82����? (3��)
 ��6����������ӿ췴Ӧ���ʣ�? (2��)
��6����������ӿ췴Ӧ���ʣ�? (2��)
��7��3.4%? (3��)
�����������
�����Ѷȣ�һ��
4��ѡ���� 2 gij��������100 ml 2 mol��L-1��������Һ�У�����ҺŨ�Ƚ���ԭŨ�ȵ�һ��ʱ������Һ������䣩��������û��Ӧ�꣬�ý���������?��?��
A��Al
B��Zn
C��Fe
D��Mg
�ο��𰸣�A
�����������
�����Ѷȣ�һ��
5��ʵ���� ��10�֣�
��1��Ũ�����ľ̿(C)����ʱ��Ӧ�Ļ�ѧ����ʽΪ��
?��
Ϊ����֤��Ӧ��ȫ�����������ͼװ�ý���ʵ�顣

��2����ͼA�������ʵ��ı�Ҫװ�ã���������ͼ�еģ����ţ�?��

��3�� Cװ����ʢ�ŵ��Լ�Ϊ?��
��������?��
��4���ܹ�֤������CO2�����ʵ�������ǣ�
?��
�ο��𰸣���1��C + 2H2SO4(Ũ)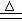 CO2�� + 2SO2�� + 2H2O����2�֣�
CO2�� + 2SO2�� + 2H2O����2�֣�
��2���ۣ�2�֣�
��3������KMnO4��Һ��2�֣�?��ȥSO2����2�֣�
��4��C������KMnO4��Һ����ɫ��ͬʱD�г���ʯ��ˮ����ǡ���2�֣�
����������ɷ�ӦC + 2H2SO4(Ũ) CO2�� + 2SO2�� + 2H2O֪��������CO2��SO2�ļ�������ж���Ҫˮ��Һ���ʲ������ʱ�����ȼ���ˮ��һ������ˮ����ͭ��
CO2�� + 2SO2�� + 2H2O֪��������CO2��SO2�ļ�������ж���Ҫˮ��Һ���ʲ������ʱ�����ȼ���ˮ��һ������ˮ����ͭ��
��CO2��SO2��Ϊ��������������������SO2���л�ԭ�ԡ�Ư���ԣ��Ƕ������ʣ��ʿ���Ʒ����Һ���������Ĵ��ڣ���������KMnO4��Һ�������գ�����ó���ʯ��ˮ����CO2�Ĵ��ڡ�
�����Ѷȣ�һ��