1、推断题 短周期元素U、V、W、X、Y原子序数递增,V、W、X、Y四种元素依次相邻,可组成U2X、WU3、VU4型10电子化合物,也可组成U2Y、U2X2、W2U4、V2U6型18电子化合物。请据各情景回答问题。
(1)上述两种相对分子质量相等的18电子化合物在水溶液中相互反应,生成一种固体单质。写出有关化学方程式:______________ 。
(2)WU3在NaClO溶液中生成W2U4,写出有关离子方程式_____________ 。
(3)U2X2和W2U4常温下均是无色液体,相互反应生成两种气体产物,均是大气成分。在pkPa、t℃时测得每生成36g U2X放出320kJ热量。写出有关热化学方程式:______________ 。
(4)W2U4-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。电池放电时:负极的电极反应式是_______________ 。
参考答案:(1)H2O2 + H2S == S↓+ 2H2O?
(2)2NH3 +ClO- == N2H4 + Cl- + H2O
(3)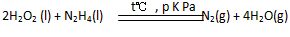 △H=-640 kJ/mol
△H=-640 kJ/mol
(4)N2H4+4OH--4e-==4H2O+N2↑
本题解析:
本题难度:一般
2、选择题 下列实验过程中,始终无明显现象的是
? [? ]
A.SO2通入BaCl2溶液中
B.CO2通入饱和Na2CO3 溶液中
C.NH3通入FeCl3溶液中
D.Cl2通入KI溶液中
参考答案:A
本题解析:
本题难度:简单
3、选择题 下列实验过程中,始终无明显现象的是
[? ]
A.NO2通入FeSO4溶液中
B.CO2通入CaCl2溶液中
C.NH3通入AlCl3溶液中
D.SO2通入已酸化的Ba(NO3)2溶液中
参考答案:B
本题解析:
本题难度:简单
4、选择题 受到光照或受热时,观察到盛浓硝酸的试剂瓶中充满红棕色的气体,据此现象可知浓硝酸发生了分解,生成物中有红棕色的NO2.经理论分析,产物中还有H2O和另外一种产物.用以下式子描述这一变化:HNO3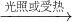 NO2+□+H2O.□内的物质可能是
NO2+□+H2O.□内的物质可能是
A.N2
B.N2O
C.NO
D.O2
参考答案:D
本题解析:分析:根据质量守恒定律,在化学反应中,反应前后原子的种类没有改变,数目没有增减,原子的质量也没有改变.根据化学方程式和质量守恒定律就可计算出生成物各元素的原子个数与反应物各元素的原子个数之差,就是未知的化学式中含有的元素的原子个数;
解答:根据质量守恒定律,反应前:氢原子:4,氮原子:4,氧原子:12;反应后,氢原子:4,氮原子:4,氧原子:10,□中的化学式中应含有H的个数为:4-4=0,应含有氮原子的个数为:4-4=0,应含有氧原子的个数为12-10=2,故□中的化学式为O2;
故选D.
点评:根据反应的化学方程式,利用反应前后原子种类、数目不变,可推断反应中某物质的分子构成、确定该物质的化学式.
本题难度:一般
5、选择题 试管中充满某气体后倒立于盛水的水槽中,试管中立即充满液体,结果如右图所示,该试管中原来所装的气体可能是( )
A.CO2
B.NO
C.NH3
D.Cl2
