| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学必考知识点《化学反应进行的方向》高频试题强化练习(2019年最新版)(四)
参考答案:A 本题解析:若发生的反应焓变小于0,反应的熵变大于0,则反应能够自发进行,即:△H<0、△S>0。因此选项是A。 本题难度:一般 2、计算题 高温时空气中的N2和O2会反应生成NO而污染大气:N2(g) +O2(g)=2NO(g)。试通过计算说明在1 200℃ 的条件下,此反应能否正向自发进行?估算此反应自发进行的最低温度是多少? 参考答案:在1 200℃的条件下此反应不能自发进行,自发进行的最低温度是7 287K。 本题解析: 本题难度:一般 3、填空题 在与外界隔离的体系中,自发过程将导致体系的________增大,这个原理也叫做________原理。在用来判断过程的方向时,就称为________判据。不难理解,即使是同一物质,应该存在着________时的熵值最大,________时次之,________时最小的这样一种普遍规律。 参考答案:熵;熵增;熵;气态;液;固 本题解析: 本题难度:一般 4、选择题 已知工业上真空炼铷的反应方程式为:2RbCl + Mg |
参考答案:D
本题解析:略
本题难度:一般
5、填空题 (6分)反应物与生成物均为气态的某可逆反应在不同条件下的反应历程分别为A、B,如图所示。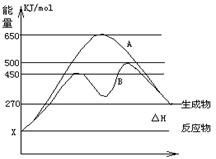
(1)据图判断该反应是______(填“吸”或“放”)热反应,当反应达?到平衡后,其他条件不变,升高温度,反应物的转化率?__? (填“增大”、“减小”或“不变”)
(2)其中B历程表明此反应采用的条件为___??(选填下列序号字母),作出正确的判断的理由为 ?
A、升高温度? B、增大反应物的浓度? C、降低温度? D、使用了催化剂
(3)若△H的数值为200KJ/mol,则x值应为 _?__KJ/mol. 此反应在A反应历程中的正反应的活化能为? _____KJ/mol,
此反应在A反应历程中的正反应的活化能为? _____KJ/mol,
参考答案:(1)?吸?;?增大? (2)? D? ;?使用催化剂能降低反应物的活化能?
(3)? 70?;? +580
本题解析:(1)由图像可知,反应物的总能量低于生成物的总能量,所以使吸热反应。升高温度平衡向正反应方向移动,转化率增大。
(2)b曲线和a曲线相比,活化能降低,说明使用了催化剂,因为使用催化剂能降低反应物的活化能,答案选D。
(3)反应热是生成物的总能量和反应物的总能量的差值,即270KJ/mol-X=200KJ/mol,则X=70KJ/mol。根据图像可知,活化能是650KJ/mol-70KJ/mol=580KJ/mol.
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点归纳《反应速率与.. | |