1��ѡ���� �������ӷ���ʽ������ȷ����
A���ö��Ե缫��������Ȼ��ƣ�
B��������������Һ��ȥ�����������Ĥ��
C��Ca(HCO3)2��Һ������NaOH��Һ���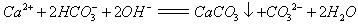
D����ʳ�׳�ȥˮƿ�е�ˮ����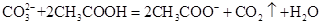
�ο��𰸣�B
���������A������ȷΪ��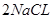 ====
====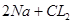 ��B��ȷ��C������ȷΪ��
��B��ȷ��C������ȷΪ��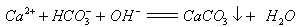 ��D����̼���Ϊ������ˮ�����ʣ����ܲ��������ʽ��
��D����̼���Ϊ������ˮ�����ʣ����ܲ��������ʽ��
�����Ѷȣ�һ��
2��ѡ���� ������Һ�еķ�Ӧ�������ӷ���ʽH����OH��=?H2O��ʾ����
A��2NaOH��CO2=Na2CO3��H2O
B��NH3��H2O��HCl =NH4Cl��H2O
C��Mg(OH)2��2HCl =MgCl2��H2O
D��2KOH��H2SO4=K2SO4��2H2O
�ο��𰸣�D
���������ϡ��ǿ����ǿ�Ӧ���ɿ������κ�ˮ�����ӷ�Ӧ�������ӷ���ʽH��+OH��=H2O��ʾ��CO2��H2O�γ�����H2CO3��NH3��H2O��Mg(OH)2�������ֻ��Dѡ����ȷ��
�����Ѷȣ�һ��
3��ѡ���� �������ӷ���ʽ��д��ȷ���ǣ�������
A���������Fe+2H+�TFe3++H2��
B��ʯ��ʯ�����CO
+2H+�TH2O+CO2��
C��ͭ����������Һ��Cu+Ag+�TCu2++Ag
D������������Һ�������ƣ�Ba2++SO�TBaSO4��
�ο��𰸣�A���������ᷴӦ��Ӧ�����Ȼ���������������ȷ�����ӷ���ʽΪFe+2H+�TFe2++H2������A����
B��̼����������������Ȼ��ơ�ˮ�Ͷ�����̼��̼��ơ�ˮ��������̼Ӧ��д��ѧʽ�������ӷ�ӦΪCaCO3+2H+�TCa2++CO2��+H2O����B����
C��ͭ�Ľ�����ǿ����������ͭ����������Һ��Ӧ��������ͭ������Cu+Ag+�TCu2++Ag����ʽ���ҵ�ɲ��غ㣬��ȷ�����ӷ�Ӧ����ʽΪCu+2Ag+�TCu2++2Ag����C����
D������������Һ���������������ᱵ���������ƣ����ᱵ������ˮ�����ӷ�Ӧ����ʽ��д��ѧʽ�����ӷ�ӦΪBa2++SO42-�TBaSO4������D��ȷ��
��ѡ��D��
���������
�����Ѷȣ���
4��ѡ���� ���з�Ӧ�����ӷ���ʽ��ȷ���ǣ�?��
A�����ˮ�еμӱ���FeCl3��Һ�Ʊ�Fe(OH)3���壺Fe3++3H2O==Fe(OH)3+3H+
B����NaHCO3��Һ��������Ca(OH)2��Һ��Ca2++OH-+HCO3-=CaCO3��+H2O
C����������Һ��̼��������Һ��ϣ�Al3++3HCO3-=Al(OH)3��+3CO2��
D���������еμӰ�ˮ��H++OH-=H2O
�ο��𰸣�C
�����������
�����Ѷȣ���
5��ѡ���� ��֪NH4����AlO2����2H2O��Al(OH)3����NH3��H2O�����е����ʵ�����NH4Cl��AlCl3��HCl�����Һ�������μ�NaOH��Һ������,�����Ͻ��裬���ܷ����������ӷ�Ӧ����H����OH����H2O����Al(OH)3��OH����AlO2����2H2O����Al3����3OH����Al(OH)3������NH4����OH����NH3��H2O����NH4����AlO2����2H2O��Al(OH)3����NH3��H2O������ȷ�����ӷ�Ӧ˳����
A���٢ۢڢ�
B���٢ۢڢ�
C���٢ۢܢ�
D���٢ܢۢ�
�ο��𰸣�C
���������H����Al3����NH�����OH����������H����Al3����NH4��������ΪNH4����AlO2����2H2O��Al(OH)3����NH3��H2O�����NH4�����OH��������ǿ�����������ģ��������е����ʵ�����NH4Cl��AlCl3��HCl���?��Һ�������μ�NaOH��Һ������,������Ӧ���Ⱥ�˳����H����OH����H2O��Al3����3OH����Al(OH)3����NH4����OH����NH3��H2O��Al(OH)3��OH����AlO2����2H2O����ѡC��4Cl��AlCl3��HCl�����Һ������������Һ��Ӧ���ӷ���ʽ�������ж�
�����Ѷȣ�һ��