|
高考化学知识点整理《化学基本概念》考点特训(2019年冲刺版)(二)
2019-06-25 21:32:33
【 大 中 小】
|
1、选择题 下列变化需要加入还原剂才能实现的是
A.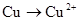
B.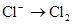
C.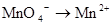
D.
|
参考答案:C
本题解析:根据氧化还原反应中还原剂所含元素的化合价升高,氧化剂所含元素的化合价降低。题中要求选择加入还原剂才能实现的过程,选项中的元素化合价应该降低,所以C正确。
考点:氧化还原反应。
本题难度:一般
2、填空题 (15分)铜及其化合物与生产、生活关系密切。
(1)用新制Cu(OH)2与葡萄糖反应制备Cu2O,该反应中葡萄糖是 (填“氧化剂”或“还原剂”)
(2)用H2O2稀硫酸共同浸泡废印刷电路板可制备CuSO4若将该反应设计成原电池,
正极的电极反应式为
(3)用NH4NO3氧化海绵铜(含Cu和CuO)生产CuCl的部分流程如下:
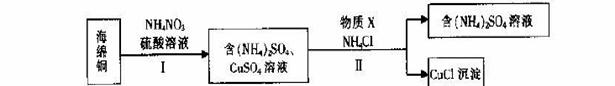
①步骤I中,反应温度不宜过高的原因是 。
②步骤I中,0.5 mol NH4NO3参加反应有4mol电子转移,铜参与反应的离子方程式为 。
③步骤II中,物质X可选用的物质是 。(填序号)。
a.Cu b.C12 c.H2O2 d.(NH4)2SO3
④步骤II中物质X需要过量的原因,其一是加快反应速率,其二是 _。
⑤步骤II中当NH4 Cl加到一定的量时,生成CuCl 会部分溶解生成CuCl2-在一定温度下建立两个平衡:
Cu Cl(s) 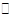 Cu+(a q) + Cl-(a q) Ksp=1.4x10-6 Cu+(a q) + Cl-(a q) Ksp=1.4x10-6
Cu Cl(s) + Cl一(a q)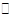 CuCl2(a q) K=0.35 CuCl2(a q) K=0.35
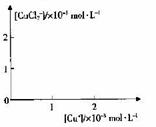
分析[Cu+]、[CuCl2-]和Ksp,K的数学关系,在图中画出「Cu+]、[CuCl2]-的关系曲线(要求至少标出坐标点)
参考答案:(1)还原剂 (2)H2O2+2e-+2H+=2H2O
(3)①防止产生氮氧化物造成污染
②4Cu+NO3-+10H+=4Cu2++NH4++3H2O ③ad ④防止CuCl被氧化
⑤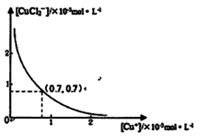
本题解析:(1)用新制Cu(OH)2与葡萄糖反应制备Cu2O,铜元素由+2价得电子生成+1价的Cu2O,作氧化剂,该反应中葡萄糖是还原剂。
(2)用H2O2稀硫酸共同浸泡废印刷电路板可制备CuSO4,若将该反应设计成原电池,铜失电子做负极,正极是H2O2得电子生成水,则正极的电极反应式为H2O2+2e-+2H+=2H2O。
(3)①硝酸铵受热分解生成氮氧化物,所以步骤I中,反应温度不宜过高的原因是防止产生氮氧化物造成污染,②用NH4NO3氧化海绵铜,铜失电子,NO3-得电子,0.5 mol NH4NO3参加反应有4mol电子转移,说明1molNO3-得8mol电子,氮元素由+5价降低到―3价,所以铜参与反应的离子方程式为4Cu+NO3-+10H+=4Cu2++NH4++3H2O,③步骤II是将硫酸铜还原成CuCl,铜元素由+2价降低到+1价,做氧化剂,需加入具有还原性的物质,且不引入杂质,a. Cu 和d. (NH4)2SO3具有还原性,能达到要求,b. C12和c. H2O2都具有强氧化性,不符,所以物质X可选用的物质是ad,④CuCl很不稳定,容易被氧化,步骤II中物质X需要过量的原因,其一是加快反应速率,其二是防止CuCl被氧化,
⑤根据①Cu Cl(s) 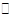 Cu+(a q) + Cl-(a q) Ksp=1.4x10-6, ② Cu Cl(s) + Cl一(a q) Cu+(a q) + Cl-(a q) Ksp=1.4x10-6, ② Cu Cl(s) + Cl一(a q)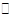 [CuCl2]-1(a q) K=0.35 ,①+②得2Cu Cl(s) [CuCl2]-1(a q) K=0.35 ,①+②得2Cu Cl(s) 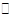 Cu+(a q)+ [CuCl2]-(a q) K=0.49×10-6,根据方程式可知:c(Cu+)・c([CuCl2]-)=0.49×10-6,两离子浓度成反比,两离子浓度相同时为0.7×10-3mol/L,据此可画出图像为: Cu+(a q)+ [CuCl2]-(a q) K=0.49×10-6,根据方程式可知:c(Cu+)・c([CuCl2]-)=0.49×10-6,两离子浓度成反比,两离子浓度相同时为0.7×10-3mol/L,据此可画出图像为:

考点:考查葡萄糖的化学性质,用NH4NO3氧化海绵铜(含Cu和CuO)生产CuCl的工艺流程,化学图像的绘制。
本题难度:困难
3、选择题 下列物质由于发生化学反应,既能使溴水褪色,又能使酸性KMnO4溶液褪色的是
A.乙烷
B.甲苯
C.乙烯
D.苯
参考答案:C
本题解析:乙烯中含有碳碳双键,能和溴水发生加成反应,也能和酸性高锰酸钾溶液发生氧化反应,所以答案选C。
本题难度:一般
4、选择题 下列物质中,不能跟金属钠反应放出氢气的是
A.汽油
B.丙醇
C.福尔马林
D.丁酸
参考答案:A
本题解析:分析:跟钠反应的物质有羧酸、醇、酚、水和酸等.
解答:A、汽油中含有烷烃,烷烃与钠不反应,故A正确;
B、丙醇与钠反应,羟基上的氢原子被还原,生成丙醇钠和氢气,故B错误;
C、福尔马林是甲醛的水溶液,钠能与水反应生成氢氧化钠和氢气,故C错误;
D、丁酸能与钠反应,羧基中的氢原子被还原,生成丁酸钠和氢气,故D错误;
故选A.
点评:本题考查了汽油、丙醇、乙酸的性质等,难度较小,以识记为主,根据所学知识来解答.
本题难度:困难
5、选择题 某元素在化学反应中由化合态变为游离态,则该元素
A.一定被氧化了
B.一定被还原了
C.既可能被还原也可能被氧化
D.既不可能被氧化又不可能被还原
|