1、选择题 实验室里利用以下反应制取少量氮气:NaNO2+NH4Cl===NaCl+N2↑+2H2O。关于该反应的下列说法正确的是
A.NaNO2是氧化剂
B.每生成1 mol N2转移的电子的物质的量为6 mol
C.NH4Cl中的氮元素被还原
D.N2既是氧化剂,又是还原剂
参考答案:A
本题解析:
A.NaNO2是氧化剂,正确,+3价的N化合价降低。
B.每生成1 mol N2转移的电子的物质的量为3mol
C.NH4Cl中的氮元素被氧化,―3价的N 化合价升高。
D.N2既是氧化产物,又是还原产物。
本题难度:困难
2、选择题 25℃时,amol.L-1一元酸HA与bmol.L-1NaOH等体积混合后,pH为7,则下列关系一定正确的是
A.a =b
B.a>b
C.c(A-) = c(Na+)
D.c(A-)
参考答案:C
本题解析:试题分析:若HA为强酸,a=b;若HA为弱酸,则a>b,但无论HA是强酸还是弱酸,均有电荷守恒:
c(Na+)+ c(H+)=c(A-)+ c(OH―),pH=7,c(H+)= c(OH―),所以c(A-) = c(Na+)。
考点:离子浓度比较
点评:本题可直接根据电荷守恒解答。
本题难度:简单
3、选择题 将12mol/L的盐酸(ρ=1.19g/cm3)50mL稀释成6mol/L的盐酸(ρ=1.10g/cm3),需加水的体积为
A.50mL
B.50.5mL
C.55mL
D.59.5mL
参考答案:B
本题解析:由于早稀释过程中溶质是不变的,所以稀释后溶液的体积是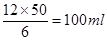 ,则稀释后溶液的质量是110g,而稀释前溶液的质量是1.19g/ml×50ml=59.5g,所以需要水的质量是110g-59.5g=50.5g,答案选B。
,则稀释后溶液的质量是110g,而稀释前溶液的质量是1.19g/ml×50ml=59.5g,所以需要水的质量是110g-59.5g=50.5g,答案选B。
本题难度:简单
4、选择题 向体积为Va的0.1mol・L-1?CH3COOH溶液中加入体积为Vb的0.1mol・L-1?KOH溶液,下列关系错误的是
A.Va>Vb时:c(CH3COOH) + c(CH3COO-)> c(K+)
B.Va=Vb时:c(CH3COOH) + c(H+) = c(OH-)
C.VaD.Va与Vb任意比时:c(K+)+ c(H+) =c(OH-)+ c(CH3COO-)
参考答案:C
本题解析:A说明醋酸是过量的,即溶液是由醋酸和醋酸钾组成的,根据原子守恒可知A正确。B说明二者恰好反应,生成的醋酸钾水解显碱性,所以根据质子守恒可知,B正确。C说明氢氧化钾是过量的,即溶液是由醋酸钾和氢氧化钾构成的,所以正确的顺序为c(K+)>c(CH3COO-) > c(OH-)>(H+),C不正确。根据电荷守恒可知,选项D是正确的。答案选C。
本题难度:简单
5、选择题 下列变化中,需加入还原剂的是
A.SO32-→SO2
B.S2-→S
C.CO2→H2CO3
D.CO2→CO
参考答案:D
本题解析:
本题难度:困难