1��ѡ���� ����������ȷ����(? )
A�����͵�ʳ��ˮ��ͨ��HCl������а�ɫ��������
B��ͬŨ�ȵ�(NH4)2SO4��(NH4)2CO3��NH4Cl��NH4HSO4��Һ�У�c(NH4+)��С
C������������ְ�ɫ��������ԭ��Һ��һ����Ag+
D�������ܽ�Al(OH)3�����ܽ�H2SiO3����Һ���Դ�������NO3-��HCO3-��I-��K+
�ο��𰸣�A
���������A������Һ�д��ڳ����ܽ�ƽ�⣬NaCl(s)  Na+(aq)+Cl-(aq)��ͨ��HCl��������Ũ�����ӣ�ƽ�������ƶ�������NaCl���壬��ȷ��B��NH4HSO4�У���Һ�����ԣ���������ˮ�⣬��Ũ�ȴ���NH4Cl��Ũ�ȣ�����C����һ�����������������ӽ�����ɹ����ɫ����������D������ҺΪ������Һ��̼��������ܴ������棬����
Na+(aq)+Cl-(aq)��ͨ��HCl��������Ũ�����ӣ�ƽ�������ƶ�������NaCl���壬��ȷ��B��NH4HSO4�У���Һ�����ԣ���������ˮ�⣬��Ũ�ȴ���NH4Cl��Ũ�ȣ�����C����һ�����������������ӽ�����ɹ����ɫ����������D������ҺΪ������Һ��̼��������ܴ������棬����
�����Ѷȣ�һ��
2��ѡ���� ���и���ɫ����ˮ��Һ�У��ܴ���������������ǣ�������
A��Na+��Mg2+��NO3-��Cl-
B��Al3+��K+��OH-��NO3-
C��Na+��Ba2+��Cl-��SO42-
D��H+��K+��SO42-��Fe3+
�ο��𰸣�A�����������֮�䲻��Ӧ������ˮ�о�Ϊ��ɫ����A��ȷ��
B����Al3+��OH-�ܽ�����������������������ܴ������棬��B����
C����Ba2+��SO42-�ܽ���������ᱵ���������ܴ������棬��C����
D�����������֮�䲻��Ӧ���ܴ������棬��Fe3+��ˮ��Ϊ��ɫ������ɫ��Һ��������D����
��ѡA��
���������
�����Ѷȣ�һ��
3��ѡ���� ��������ʵ���ó��Ľ��ۻ�����Ľ�����ȷ����
?
| ʵ����ʵ
| ���ۻ����
|
A
| ��40 g NaOH����1 L����ˮ��
| ����Һ�����ʵ���Ũ��Ϊ1mol�qL-1
|
B
| 0.1 mol/L CH3COOH��Һ��ϡ������
| 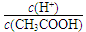 ?����С ?����С
|
C
| ��H2X����
| �����£���NaHX��ҺpHһ������7
|
D
| ����Һ��ϡ������
| ����Ũ�ȣ��еĿ��������еĿ��ܼ�С���еĿ��ܲ���
�ο��𰸣�D
���������A����ȷ����Ϊ����ȷ����Һ�������������������ʣ�ϡ�ʹٽ����롣��ϡ�����������ӵ����ʵ������ӣ�������ӵ����ʵ������٣�����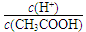 �����B����ȷ��C����ȷ�����HX���ĵ���̶ȴ���ˮ��̶ȣ���Һ�����ԣ������ȷ�Ĵ�ѡD�� �����B����ȷ��C����ȷ�����HX���ĵ���̶ȴ���ˮ��̶ȣ���Һ�����ԣ������ȷ�Ĵ�ѡD��
�����������Ǹ߿��еij�����������ͣ������е��Ѷ�����Ŀ��飬�����ۺ���ǿ����ע�ض�ѧ������֪ʶ���̺�ѵ����ͬʱ�����ض�ѧ������������������ּ�ڿ���ѧ��������û���֪ʶ���ʵ�����������������������ѧ���������������ͳ���˼ά���������ѧ����ѧϰЧ�ʺ�Ӧ��������
�����Ѷȣ�һ��
4������� ��15�֣�����A��B��C��D��E��F���ֳ��������� ����Ϊǿ����ʣ����ǵ���������Al3+��NH+4��Na+��Ag+��H+���֣���������Cl-��HCO-3��OH-��NO-3��SO2-4���֣��ֽ����Ƿֱ����0.lmol/L������Һ����������ʵ�飺 ����Ϊǿ����ʣ����ǵ���������Al3+��NH+4��Na+��Ag+��H+���֣���������Cl-��HCO-3��OH-��NO-3��SO2-4���֣��ֽ����Ƿֱ����0.lmol/L������Һ����������ʵ�飺
�ٲ��A��Һ�ʼ��ԣ�E��Һ��pHΪ1��C��Һ������ǿ��E��Һ��
����B��Һ�е���D��Һ�����ְ�ɫ��������ɫ��ζ���壬�ð�ɫ������������A��Һ����������C��Һ�����ˣ�����Һ�м���A��Һ�����ȣ��д̼�����ζ���������
����B��Һ�еμ�F��Һ��������ɫ�������������E��Һ���������ܽ⡣
����E��Һ�еμ�F��Һ�������Ա仯��
��������ʵ�����ش��������⣺
��1��д���������ֻ�����Ļ�ѧʽ��
A ��B ��D ��F ��
��2��C��Һ�� ���ж�������____
��3��B��D��Ӧ�����ӷ���ʽ��____ ��
�ο��𰸣�(15��)
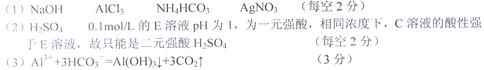
�����������
�����Ѷȣ�һ��
5��ѡ���� ������������Һ�л����ڼ�����Һ�У����ܴ����������������
A��Na+��Ba2+��S2-��SO42-
B��Na+��K+��SO42-��Cl-
C��SO42-��Ba2+��Cl-��K+
D��K+��NO3-��Ca2+��CO32-
�ο��𰸣�B
���������A����Ba2+��SO42-���ܹ��棻B��ȷ��C����Ba2+��SO42-���ܹ��棻D����Ca2+��CO32���ܹ��棬������ȷ�Ĵ�ѡB��
�����Ѷȣ���
|