1、选择题 X、Y、Z、M代表四种金属元素。金属X和Z用导线连接放入稀硫酸中时,X溶解,Z极上有氢气放出;若电解Y2+和Z2+离子共存的溶液时,Y先析出;又知M2+离子的氧化性强于Y2+离子。则这四种金属的活动性由强到弱的顺序为
A.M>Z>X>Y
B.X>Y>Z>M
C.X>Z>Y>M
D.X>Z>M>Y
参考答案:C
本题解析:金属X和Z用导线连接放入稀硫酸中时,X溶解,Z极上有氢气放出,表明活动性X>Z;若电解Y2+和Z2+离子共存的溶液时,Y先析出,表明活动性Z>Y;M2+离子的氧化性强于Y2+离子,表明活动性Y>M,综述,X>Z>Y>M,C正确。
本题难度:一般
2、选择题 下图甲和乙是双液原电池装置。由图可判断下列说法错误的是
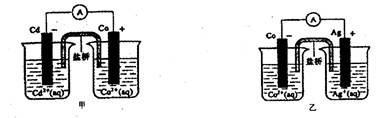
A.甲图电池反应的离子方程式为: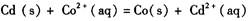
B.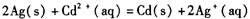 反应能够发生
反应能够发生
C.盐桥的作用是形成闭合回路,并使两边溶液保持电中性
D.乙图当有Imol电子通过外电路时,正极有108克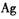 析出
析出
参考答案:B
本题解析:略
本题难度:一般
3、填空题 将0.23 mol SO2和0.11 mol O2放入容积为1 L的密闭容器中,发生反应2SO2+O2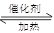 2SO3,在一定温度下,反应达到平衡,得到0.12 mol SO3,则反应的平衡常数K=?。若温度不变,再加入0.50 mol氧气后重新达到平衡,则SO2的平衡浓度??(填“增大”“不变”或“减小”),氧气的转化率??(填“升高”“不变”或“降低”),SO3的体积分数??(填“增大”“不变”或“减小”)。
2SO3,在一定温度下,反应达到平衡,得到0.12 mol SO3,则反应的平衡常数K=?。若温度不变,再加入0.50 mol氧气后重新达到平衡,则SO2的平衡浓度??(填“增大”“不变”或“减小”),氧气的转化率??(填“升高”“不变”或“降低”),SO3的体积分数??(填“增大”“不变”或“减小”)。
参考答案:23.8 mol-1・L 减小 降低 减小
本题解析:2SO2+O2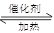 2SO3平衡时,各物质浓度分别为0.11mol/L、0.05mol/L、0.12mol/L,
2SO3平衡时,各物质浓度分别为0.11mol/L、0.05mol/L、0.12mol/L,
依据平衡常数的概念K= 23.8 mol-1・L
23.8 mol-1・L
再加入氧气0.50 mol,平衡右移,平衡后SO2的平衡浓度减小,但氧气本身的转化率减小
由于混合物的总物质的量增加的程度远大于新生成的SO3,故SO3在混合气体中的体积分数反而减小
本题难度:一般
4、填空题 如图所示,甲、乙两装置电极材料都是铁棒与碳棒,请回答下列问题:
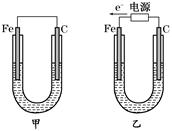
(1)若两装置中均为CuSO4溶液,反应一段时间后:
①有红色物质析出的是甲装置中的 棒,乙装置中的 棒。
②乙装置中阳极的电极反应式是: 。
(2)若两装置中均为饱和NaCl溶液:
①写出乙装置中总反应的离子方程式: 。
②甲装置中碳极的电极反应式是 ,乙装置碳极的电极反应属于 (填“氧化反应”或“还原反应”)。
③将湿润的淀粉KI试纸放在乙装置碳极附近,发现试纸变蓝,解释其原因: 。
参考答案:(1)①碳 铁 ②4OH--4e-=2H2O+O2↑
(2)①2Cl-+2H2O Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
②2H2O+O2+4e-=4OH- 氧化反应
③在乙装置碳棒电极上生成Cl2,Cl2与I-反应生成I2,I2遇淀粉变蓝
本题解析:甲为原电池,乙为电解池。
(1)若两装置中均为CuSO4溶液,则:
甲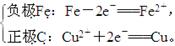
乙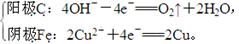
(2)若均为NaCl溶液,则:
甲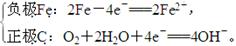
乙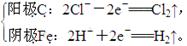
本题难度:一般
5、填空题 (10分)Zn-Cu-H2SO4原电池的负极材料是是?,正极反应式是?,发生?反应(填反应类型),总反应式为___________________________________。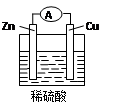
参考答案:Zn? 2H++2e-=====H2↑?还原反应? Zn+2H2SO4=====ZnSO4+2H2↑(10分)
本题解析:活泼金属做负极,相对不活泼的金属做正极,总反应Zn+2H2SO4=====ZnSO4+2H2↑
本题难度:简单