1、实验题 现用质量分数为98%,密度为1.84g/cm3的浓硫酸来配制500ml 0.2mol/L的稀硫酸,可供选择的仪器有:
①玻璃棒 ②烧杯 ③胶头滴管 ④量筒 ⑤容量瓶 ⑥托盘天平⑦药匙
(1)上述仪器中,配制过程中用不到的有___________ 。
(2)计算所需浓硫酸的体积为__________ 。现有①10ml ②50ml ③100ml三种规格的量筒,最好选用__________ 。(填代号)
(3)在配制过程中,下列操作可引起所配溶液浓度偏高的有____________ 。(填代号)
①洗涤量取浓硫酸的量筒,并将洗涤液转移到定量瓶中。
②未等稀释后的硫酸溶液冷却至室温就转移到容量瓶中
③转移前,容量瓶中含有少量蒸馏水
④未洗涤稀释浓硫酸时用过的烧杯和玻璃棒
⑤定容量,俯视刻度线
2、选择题 向体积均为10 mL且物质的量浓度相同的两份NaOH溶液中分别通入一定量的CO2得到溶液
甲和乙;向甲、乙两溶液中分别滴加0.1mol・L-1盐酸,此时反应生成CO2体积(标准状况) 与所加盐酸体积间的关系如图所示。则下列叙述中正确的是( ?)
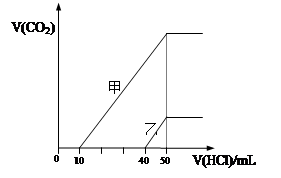
A.原NaOH溶液的物质的量浓度为0.5 mol・L-1
B.当0<V(HCl)<10mL时,甲溶液中发生反应的离子方程式为: OH-+H+=H2O
C.乙溶液中含有的溶质是NaOH、NaHCO3
D.乙溶液中滴加盐酸后产生CO2体积的最大值为112mL(标准状况)
3、选择题 小明体检的血液化验单中,葡萄糖为5.9×10-3 mol・L-1 。表示该体检指标的物理量是
A.溶解度(s)
B.物质的量浓度(c)
C.质量分数(w)
D.摩尔质量(M)