1、填空题 下图表示一些晶体中的某些结构,它们分别是NaCl、CsCl、干冰、金刚石、石墨结构中的某一种的某一部分。
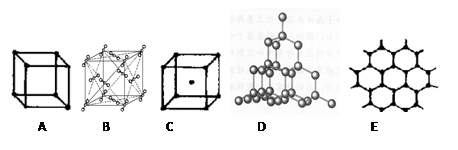
(1)代表金刚石的是(填编号字母,下同)?,金刚石中每个碳原子与?个碳原子最接近且距离相等。金刚石属于?晶体;
(2)代表石墨是?,其中每个正六边形占有的碳原子数平均为?个;
(3)代表干冰的是?,它属于?晶体,每个CO2分子与?个CO2分子紧邻;
(4)上述B、C、D三种物质熔点由高到低的排列顺序为?。
参考答案:(10分)(1)D,4,原子?(2)E, 2?(3)B,分子,12?(每空1分)
(4)金刚石>CsCl>干冰(2分)
本题解析:(1)金刚石是原子晶体,则代表金刚石的是选项D;金刚石中每个碳原子与4个碳原子最接近且距离相等。
(2)石墨是层状结构,则代表石墨的是选项E。石墨中碳原子被相邻的3个正六边形共用,则每个正六边形占有的碳原子数平均为6÷3=2个。
(3)干冰是分子晶体,则代表代表干冰的是选项B,每个CO2分子与(3×8)÷2=12个CO2分子紧邻。
(4)C是氯化铯,形成的晶体是离子晶体,则B、C、D三种物质熔点由高到低的排列顺序为金刚石>CsCl>干冰。
点评:该题是基础性试题的考查,试题紧扣教材基础知识,有利于调动学生的学习兴趣和学习积极性,旨在巩固学生的基础,提高学生灵活运用基础知识解决实际问题的能力,有利于培养学生的抽象思维能力和空间想象能力。
本题难度:一般
2、选择题 下列说法正确的是
A.全部由非金属元素形成的化合物中只含有共价键
B.分子晶体的熔点较低,因为分子晶体中有化学键
C.金属在常温下都以晶体形成存在
D.金属晶体中,自由电子几乎均匀分布在整个晶体中,被许多金属离子共用
参考答案:D
本题解析:略
本题难度:简单
3、填空题 下图是元素周期表的一部分
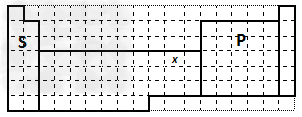
⑴表中区域名称s、p……等确定的依据是____________________________。 ?
⑵已知A原子的M层和N层的电子数分别比B原子的M层和N层的电子数少7个和4个,则A的核外电子排布式为______________,B在元素周期表中的位置是___________。
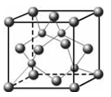
⑶上表中元素x的一种氢化物的晶体结构如图所示,写出该化合物在氯气中燃烧的化学方程式__________。除x外,第四周期中最外层只有一个电子的还有_________(填元素名称)。
⑷表中短周期非金属元素之间可以形成形形色色的有机物,如邻羟基苯甲醛(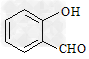 )和对羟基苯甲醛(
)和对羟基苯甲醛( ),前者沸点低于后者,理由是___________________。
),前者沸点低于后者,理由是___________________。
参考答案:⑴根据构造原理最后填入电子的能级的符号
⑵1s22s22p63s23p63d34s2;第四周期第VIA
⑶2CuH+3Cl2==2CuCl2+2HCl;钾、铬
⑷邻羟基苯甲醛存在分子内氢键,而对羟基苯甲醛存在分子间氢键
本题解析:
本题难度:一般
4、填空题 (16分)观察下列部分图形,并按要求回答下列问题
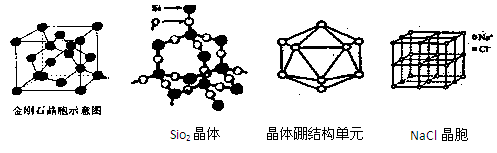
(1)由金刚石晶体结构和晶胞图知,金刚石是原子晶体,晶体中碳原子取?
杂化轨道形成σ键,每个晶胞中含碳原子数为?个。
(2)白磷分子(P4)中键角为?,分子的空间结构为?,每1mol白磷分子含?mol P-P共价键。若将1分子白磷中所有P-P键打开并各插入一个氧原子所得氧化物的分子式为?,若每个P原子的孤对电子再与氧原子配位,就可得到磷的另一种氧化物?(填分子式)。
(3)由SiO2晶体结构知SiO2晶体是?晶体,每1mol SiO2晶体含?mol Si-O共价键。
(4)已知CaC2晶体的晶胞结构与NaCl晶体相似,(如图)但CaC2晶体中哑铃形C22-的存在,使晶胞沿一个方向拉长,则CaC2晶体中Ca2+配位数(C.N)为?。C22-与O22+互为等电子体,O22+的电子式为?,1molO22+中含π键数目为?。
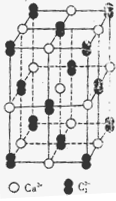
(5)晶体硼的基本结构单元都是由硼原子组成的正二十面体的原子晶体。其中含有20个等边三角形和一定数目的顶角,每个顶角各有一个原子,观察图形回答。这个基本结构单元由?个硼原子组成,共含有?个B-B键。
(6)若测得mg NaCl固体的体积为Vcm3,已知NaCl晶体中,靠得最近的Na+、Cl-间的距离为a cm,则阿佛加德罗常数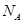 的表达式为?。
的表达式为?。
参考答案:(16分)(1)SP3,???8?。
(2)60°, ?正四面体,6 ,?P4O6,???P4O10? .
(3)原子,? 4。
(4)? 4 ?、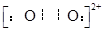 ??、? 2NA个?。
??、? 2NA个?。
(5)? 12?、 30??。
(6)?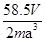 ?。(除(6)2分,其余每空1分)
?。(除(6)2分,其余每空1分)
本题解析:略
本题难度:一般
5、选择题 有四种晶体,其离子排列方式如下图所示,其中化学式不属AB型的是(?)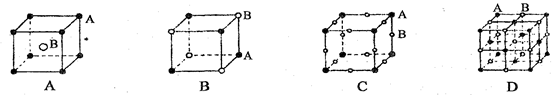
参考答案:D
本题解析:AB型堆积为六方最密堆积,而D为体心立方堆积,因此错误。
本题难度:一般