1、选择题 下列有关配合物的论述不合理的是( )
A.Na[Al(OH)4]和[Ag(NH3)2]OH都是配合物
B.Na3[AlF6]、Na2[SiF6]和[Cu(NH3)4]Cl2的配位数都是6
C.[ZnCl4]2-的空间构型为正四面体形
D.配合物[Cr(H2O)4Br2]Br?2H2O中,中心离子的化合价为+3价,配离子带1个单位的正电荷
参考答案:B
本题解析:
本题难度:简单
2、填空题 指出下列各配合物中的配离子、中心离子、配位体、配位数及配位原子。
(1)K2[Cu(CN)4]____________
(2)[Co(NH3)(en)2Cl]Cl2____________?
(3)K2Na[Co(CNO)6]____________?
(4)K2[Pt(NH3)2(OH)2Cl2]____________?
参考答案:(1)配离子为[Cu(CN)4]2-,中心离子为Cu2+,配位体为CN-,配位数为4,配位原子为C
(2)配离子为[Co(NH3) (en)2Cl]2+,中心离子为CO3+,配位体为NH3、en、Cl-,配位数为4,配位原子为N、N、Cl
(3)配离子为[Co(CNO)6]3-,中心离子为Co3+,配位体为CNO-,配位数为6,配位原子为O
(4)配离子为[Pt(NH3)2(OH)2Cl2]2-,中心离子为pt2+,配位体为NH3、OH-、Cl-,配位数为6,配位原子为N、O、Cl
本题解析:
本题难度:一般
3、填空题 (1)过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关.一般地,d0或d10排布时,无颜色,d1~d9排布时,有颜色,如[Co(H2O)6]2+显粉红色.据此判断,[Mn(H2O)6]2+______颜色(填“有”“无”).
(2)利用CO可以合成化工原料COCl2、配合物Fe(CO)5等.COCl2分子的结构式为
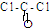
,则COCl2分子内含有______.
A.4个σ键?B.2个σ键、2个π键?C.2个σ键、1个π键?D.3个σ键、1个π键.
参考答案:(1)Mn2+离子的原子核外排布式为1s22s22p63s23p63d5,其d轨道上有5的电子,故[Mn(H2O)6]2+ 有颜色,
故答案为:有;?
(2)COCl2分子的结构式为:
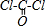
,C=O键中含有1个δ键,1个π键,则COCl2分子内含有3个σ键、1个π键,故答案为
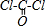
,D.
本题解析:
本题难度:一般
4、选择题 将灼热的铜丝伸入盛氯气的集气瓶中,剧烈反应,燃烧产生棕黄色烟,向集气瓶中加入少量水,观察到溶液呈黄绿色,主要原因是因为CuCl2溶液中存在黄绿色的[CuCl4]2-离子。现向蓝色的硫酸铜溶液中,加入少量稀氨水,得到蓝色絮状沉淀,继续加入氨水后,蓝色沉淀溶解,得到深蓝色溶液,再向其中加入少量浓盐酸溶液,得到绿色溶液,则该绿色溶液中主要存在的离子是
[? ]
A. Cu2+、[Cu(H2O)4]2+、SO42-
B. [CuCl4]2-、[Cu(H2O)4]2+、NH4+、SO42-
C. [CuCl4]2-、NH4+、SO42-
D. [Cu(NH3)4]2+、[Cu(H2O)4]2+、SO42-
参考答案:B
本题解析:
本题难度:一般
5、选择题 已知Co(Ⅲ)的八面体配合物CoClm nNH3,若 1mol配合物与AgNO3溶液作用生成1molAgCl 沉淀,则m、n的值是
nNH3,若 1mol配合物与AgNO3溶液作用生成1molAgCl 沉淀,则m、n的值是
[? ]
A.m=1,n=5
B.m=3,n=4
C.m=5,n=1
D.m=4,n=5
参考答案:B
本题解析:
本题难度:一般