1��ѡ���� һ����14%������������Һ��������������50 gˮ��û�������������������ʵ���������ǡ������һ���������Ϊ62.5 mL������������Һ�����ʵ���Ũ��Ϊ
A��2.2 mol / L
B��4 mol / L
C��5 mol / L
D��6.25 mol / L
�ο��𰸣�B
�������������������Һ��������m����������������������ʲ����֪����m��50g����14����m��28�������m��50g�������ʵ�������50g��28����14g�����ʵ�����14g��56g/mol��0.25mol���������������ҺŨ����0.25mol��0.0625L��4.0mol/L����ѡB��
�����Ѷȣ�һ��
2������� ��15.6g Na2O2��2.7g Al�ۻ�Ϻ�Ͷ��������ˮ�У���ַ�Ӧ�����ܲ���������ȫ���ų�����
��1��Na2O2��ˮ��Ӧ�Ļ�ѧ����ʽΪ ��15.6g Na2O2�ڸ÷�Ӧ��ת�Ƶ��ӵ����ʵ���Ϊ mol��
��2����Ӧ����ʱ���ɵ������ڱ�״����Ϊ L��
��3��ȡa g Na2O2��Al����ɵĻ�������������ˮ�У�������ȫ�ܽ⣬�ڱ�״����
�ų�����V L����V��ȡֵ��Χ�� ���ú�a�Ĵ���ʽ��ʾ������ɲ�����
�ο��𰸣�1��2Na2O2+2H2O=4NaOH+O2����0.2mol ��2��5.6L
��3��
�����������1��Na2O2��ˮ��Ӧ�Ļ�ѧ����ʽΪ2Na2O2+2H2O=4NaOH+O2�����÷�Ӧת�Ƶĵ�����Ϊ2����2molNa2O2�μӷ�Ӧ��ת�Ƶĵ�����Ϊ2mol��15.6g Na2O2Ϊ0.2mol������5.6g Na2O2�ڸ÷�Ӧ��ת�Ƶ��ӵ����ʵ���Ϊ0.2mol��2����Ӧ����ʱ���ɵ�������һ������������һ���������������������������V1=0.2/2��22.4=2.24L������NaOH�ķ�ӦΪ
2Al��2NaOH��2H2O=2NaAlO2��3H2��,�������������������V2=2.7/27��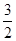 ��22.4=3.36L�����Է�Ӧ����ʱ���ɵ������ڱ�״����2.24+3.36=5.6L����3����Na2O2���ʵ���Ϊxmol ��Al ���ʵ���Ϊymol���ݣ�
��22.4=3.36L�����Է�Ӧ����ʱ���ɵ������ڱ�״����2.24+3.36=5.6L����3����Na2O2���ʵ���Ϊxmol ��Al ���ʵ���Ϊymol���ݣ�
2Na2O2+2H2O=4NaOH+O2�� 2Al2Al��2NaOH��2H2O=2NaAlO2��3H2������֪��
��ͬ������Al��Na2O2����������Ҫ�࣬���Ե�AlԽ������Խ�࣬����Ҫ������ȫ�ܽ⣬��˵�Al��Na2O2������NaOHǡ�÷�Ӧʱ������ࡣ��ʱ
78x+27y=a y��2x V����x/2��3y/2����22.4 ����x=a/132��y=2a/132������V=
�෴��AlԽ������Խ�٣���AlΪ0ʱ���������������٣���ʱ
V=22.4��x/2=��22.4��a��/��2��78��= ����ȴ���ܴﵽ������V��ȡֵ��Χ��
����ȴ���ܴﵽ������V��ȡֵ��Χ�� ��
��
���㣺Ԫ�ؼ��仯����
������ ���⿼����Ԫ�ؼ��仯����ļ��㣬����������һ�����Ѷ��ƶȣ����һ�����ѶȽϴ�
���⿼����Ԫ�ؼ��仯����ļ��㣬����������һ�����Ѷ��ƶȣ����һ�����ѶȽϴ�
�����Ѷȣ�һ��
3��ѡ���� ������������ԭ���������ǣ�������
A��7.5gC2H6
B��14gN2
C��7gCO
D��24gO2
�ο��𰸣�A��һ����������к���8��ԭ�ӣ�7.5g������ԭ������=7.5g30g/mol��8��NA/mol=2NA��
B��һ�����������к���2��ԭ�ӣ�14g������ԭ������=14g28g/mol��2��NA/mol=NA��
C��һ��һ����̼�����к���2��ԭ�ӣ�7gCO��ԭ������=7g28g/mol��2��NA/mol=0.5NA��
D��һ�����������к���2��ԭ�ӣ�24g������ԭ������=24g32g/mol��2��NA/mol=1.5NA��
ͨ�����Ϸ���֪��ԭ���������������飬
��ѡ��A��
���������
�����Ѷȣ�һ��
4��ѡ���� ��AlCl3��NaCl�Ļ����ҺVL���������ֳ����ݡ�һ�ݵμӰ�ˮ��ʹAl3+������ȫ��������һ�ݵμ�AgNO3��Һ��ʹCl��������ȫ��������Ӧ������a mol NH3��H2O��b mol AgNO3���ݴ˵�֪ԭ�����Һ�е�c(Na+) ��mol/L��Ϊ
A��(2b-4a)/V
B��(b-a)/V
C��(2b-2a)/V
D����b-2a��/V
�ο��𰸣�C
���������һ���еμӰ�ˮ��ʹAl3+������ȫ������������Ӧ����a mol NH3��H2O����n(Al3+)="a�M3" mol.n(AlCl3)=n(Al3+)="a�M3" mol. AlCl3�Ͳ�����������n(Cl��)=amol,���� ��һ�ݵμ�AgNO3��Һ��ʹCl��������ȫ����������b mol AgNO3����n(Cl��)��="b" mol.��NaCl������������n(Cl��)=(b-a)mol,n((Na+)=n(Cl��)=(b-a)mol,����c(Na+)=n((Na+)�MV�M2="(b-a)mol�MV�M2L=(2b-2a)/V(" mol/L).������ȷѡ��ΪC��
�����Ѷȣ�һ��
5��ѡ���� ����˵����ȷ����
[? ]
A��1?mol��Լ����6.02��1023����
B��1?mol?H2O�к��е���ԭ����Ϊ2NA
C���Ƶ�Ħ�����������������ԭ������
D��1?mol�������������98?g/mol
�ο��𰸣�B
���������
�����Ѷȣ���