1��ѡ���� ��NA��������٤����������ֵ������˵����ȷ����
A.32gO3��NA��O2��������ԭ������ͬ
B.NA��һ����̼���Ӻ�0.5mol�����������Ϊ7��2
C.46gNO2��46gN2O4���е�ԭ����֮��Ϊ3NA
D.2.4g����þ�����������ᷴӦ�����������ķ�����ΪNA
�ο��𰸣�B
���������������A��NA��O2��������ԭ����Ϊ2NA��������n= ��32gO3����ԭ�ӵ����ʵ������ٸ���N=nNA������ԭ����Ŀ���ݴ��жϣ�
��32gO3����ԭ�ӵ����ʵ������ٸ���N=nNA������ԭ����Ŀ���ݴ��жϣ�
B��NA��һ����̼�������ʵ���Ϊ1mol������m=nM���������������жϣ�
C���������������������������е�Ԫ�ص���������Ϊ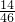 ����Ԫ�ص���������Ϊ
����Ԫ�ص���������Ϊ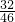 �����㵪Ԫ������Ԫ�ص�����������n=
�����㵪Ԫ������Ԫ�ص�����������n= ���㵪ԭ������ԭ�����ʵ�������ϸ���N=nNA����ԭ����Ŀ��
���㵪ԭ������ԭ�����ʵ�������ϸ���N=nNA����ԭ����Ŀ��
D��2.4g����þ�����������ᷴӦ����������0.1mol������N=nNA��������������Ŀ��
���A��NA��O2��������ԭ����Ϊ2NA����32gO3����ԭ�ӵ����ʵ���Ϊ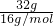 =2mol������32gO3�к�����ԭ����ĿΪ
=2mol������32gO3�к�����ԭ����ĿΪ
2mol��NAmol-1=2NA��������ȣ���A����
B��NA��һ����̼���ӵ����ʵ���Ϊ1mol������Ϊ28g��0.5mol���������Ϊ0.5mol��16g/mol=8g�����Զ�������֮��Ϊ
28��8=7��2����B��ȷ��
C���������������������������ʽ��ͬ�����������е�Ԫ�ص���������Ϊ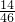 ����Ԫ�ص���������Ϊ
����Ԫ�ص���������Ϊ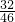 ��
��
��46gNO2��46gN2O4�����е�Ԫ������Ϊ92g��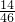 =28g����ԭ�ӵ����ʵ���Ϊ2mol����Ԫ�ص�����Ϊ92g��
=28g����ԭ�ӵ����ʵ���Ϊ2mol����Ԫ�ص�����Ϊ92g��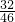 =64g��������ԭ�ӵ����ʵ���Ϊ4mol����46gNO2��46gN2O4���е�ԭ������Ϊ��2mol+4mol����NAmol-1=6NA����C����
=64g��������ԭ�ӵ����ʵ���Ϊ4mol����46gNO2��46gN2O4���е�ԭ������Ϊ��2mol+4mol����NAmol-1=6NA����C����
D������Mg+2HCl=MgCl2+H2����֪��2.4g����þ�����������ᷴӦ����������0.1mol�������ķ�����Ϊ0.1NA����D����
��ѡ��B��
���������鳣�û�ѧ�������йؼ��㣬�Ѷ��еȣ�Cѡ���д���ƽ��2NO2?N2O4��ע��������ļ��㣮
�����Ѷȣ�����
2��ѡ���� С������������������Ʒ����ơ�ʳ�Ρ�ʳ�ס�Ư�ۣ�С������������Ʒ������ɵ������ǣ�?��
A�������������̷����Ƿ���е���
B����������ˮ���Ƿ���Cl��
C����ȥ����ƿ�е�ˮ��[��Ҫ�ɷ�ΪMg(OH)2��CaCO3]
D��ϴȥ��ɫ�·��ϵĺ�ɫ����֭
�ο��𰸣�B
��������������õ�Ƽ�����۵Ĵ��ڣ����������A�������Ƿ���Cl����Ҫ��������ϡ���ᣬ�������B������ʳ�ף����д��ᣩ��ȥ����ƿ�е�ˮ�������������C������Ư��ϴȥ��ɫ�·��ϵĺ�ɫ����֭�����������D��
��������Ϥ�������ʵ����ʺͼ��鷽��
�����Ѷȣ�һ��
3������� �����и��������ʷ����Ĵ�����ĸ�����ڸ�С��ĩ�ĺ����ϣ�
A�����˷���B���ᾧ����C����Һ����D����ȡ����E������?F��������
��1����ȥʳ��ˮ�е���ɳ______��?
��2������ˮ�����͵Ļ����______��
��3����60%�ľƾ���Һ����ȡ��ˮ�ƾ�______��
��4����ȥ�Ȼ��ƹ����еĵⵥ��______��
��5��������غ��Ȼ��ƵĻ��Һ�л�������______��
��6���ӵ�ˮ����ȡ�ⵥ��______��
�ο��𰸣���1����ɳ������ˮ��Ϊ���壬���ù��˵ķ������룬�ʴ�Ϊ��A��
��2��ˮ�����ͻ������ܣ����÷�Һ�ķ������룬�ʴ�Ϊ��C��
��3��ˮ�;ƾ��ķе㲻ͬ����������ķ������룬�ʴ�Ϊ��E��
��4���������������ȿ����Ȼ��Ʒ��룬�ʴ�Ϊ��F��
��5������غ��Ȼ��Ƶ��ܽ�Ȳ�ͬ�����ýᾧ�����룬�ʴ�Ϊ��B��
��6�������л��ܼ��е��ܽ�ȱ���ˮ�д�����ȡ�ķ������룬�ʴ�Ϊ��D��
���������
�����Ѷȣ���
4��ѡ���� ijѧ������ʵ��������з�������ϴ����������ϡ����ϴ������������Ӧ���Թܣ����þƾ�ϴ��մ�б��ӵ��Թܣ����ö���̼ϴ��մ����ǵ��Թܣ���������ϴ��ʢ������ʯ��ˮ���Լ�ƿ�v?�w
A�������ⶼ��ȷ
B�������ⶼ��ȷ
C��ֻ�٢���ȷ
D��ȫ����ȷ
�ο��𰸣�D
���������ϡ�������ܽ��������������ھƾ��У�������������CS2�У�ʯ��ʯ�Լ��������ƶ��ܺ����ᷴӦ�����Դ�ѡD��
�����Ѷȣ���
5��ѡ���� ���и��������У����÷�Һ©�����з����һ�������ǣ�?��
A���ƾ���ˮ��������������������
B��������Ȼ�̼
C��ˮ�����Ȼ�̼����������������
D���Ȼ��ƺ�ˮ
�ο��𰸣�C
���������A���ƾ���ˮ���ܣ������÷�Һ©�����з��룬��A����
B��������Ȼ�̼���ܣ������÷�Һ©�����з��룬��B����
C��ˮ�����Ȼ�̼���ܣ����÷�Һ©�����з��룬��C��ȷ��
D�����ͺ�ֲ���ͻ��ܣ������÷�Һ©�����з��룬��D����
��ѡC��
�����Ѷȣ���